
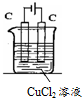
 电解氯化铜溶液的化学方程式为CuCl2$\frac{\underline{\;通电\;}}{\;}$Cu+Cl2↑.电解过程中,Cu2+离子向阴极移动;Cl-在阳极失电子,发生氧化反应(填“氧化”或“还原”).电解过程中,如果有0.4mol的电子发生转移,理论上阴极的质量将增加12.8g.
电解氯化铜溶液的化学方程式为CuCl2$\frac{\underline{\;通电\;}}{\;}$Cu+Cl2↑.电解过程中,Cu2+离子向阴极移动;Cl-在阳极失电子,发生氧化反应(填“氧化”或“还原”).电解过程中,如果有0.4mol的电子发生转移,理论上阴极的质量将增加12.8g. 分析 电解足量CuCl2溶液时,阳极上氯离子放电、阴极上铜离子放电,阳离子移向阴极,阴离子移向阳极,相当于电解氯化铜,根据转移电子和物质之间的关系式计算.
解答 解:电解足量CuCl2溶液时,阳极上氯离子放电、阴极上铜离子放电,阳离子移向阴极,阴离子移向阳极,相当于电解氯化铜,电解氯化铜溶液的化学方程式为CuCl2$\frac{\underline{\;通电\;}}{\;}$Cu+Cl2↑,反应转移电子2mol,会产生1mol金属铜,电解过程中,如果有0.4mol的电子发生转移,会产生0.2mol金属铜,理论上阴极的质量将增加0.2mol×64g/mol=12.8g.
故答案为:CuCl2$\frac{\underline{\;通电\;}}{\;}$Cu+Cl2↑;阴;阳;氧化;12.8.
点评 本题以电解原理为载体考查物质的量的计算,明确离子放电顺序及方程式中各个物理量之间的关系式即可解答,注意基础知识的积累,题目难度不大.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 组号 | 反应温度(℃) | Na2S2O3浓度(mol/L) | HCl浓度(mol/L) |
| A. | 10 | 0.1 | 0.1 |
| B. | 10 | 0.2 | 0.2 |
| C. | 20 | 0.1 | 0.1 |
| D. | 20 | 0.2 | 0.2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba2+、K+、Cl-、CO32- | B. | Na+、HCO3-、K+、OH- | ||
| C. | K+、Ag+、Cl-、NO3- | D. | Na+、SO42-、K+、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应中的能量变化,通常表现为热量的变化 | |
| B. | 反应物的总能量高于生成物的总能量时发生放热反应 | |
| C. | Ba(OH)2•8H2O与NH4Cl的反应是吸热反应 | |
| D. | 在化学反应中需要加热的反应就是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 用下列仪器、药品验证由铜和适量浓硝酸反应产生的气体中含NO(仪器可选择使用,N2和O2的用量可自由控制).
用下列仪器、药品验证由铜和适量浓硝酸反应产生的气体中含NO(仪器可选择使用,N2和O2的用量可自由控制).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卫星上的太阳能电池工作 | |
| B. | 向氢氧化铁胶体中加入稀硫酸产生红褐色沉淀 | |
| C. | 向鸡蛋清中加入饱和硫酸铵溶液,产生白色沉淀 | |
| D. | 向盛有红墨水的试管中加入活性炭,振荡,红色褪去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
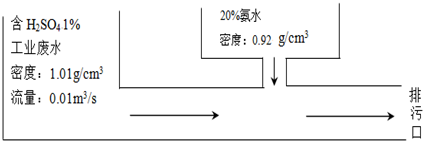
| A. | 1.98×10-3m3/s | B. | 5.49×10-4m3/s | C. | 1.90×10-4 m3/s | D. | 9.52×10-5 m3/s |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com