
某澄清、透明的浅黄色溶液中,可能含有下列八种离子:Na +、NH4+、Fe3+、Ba2+、Al3+ 、SO42-、HCO3- 、I-,在设计检验方案前的初步分析中,可确定该溶液中能大量存在的离子最多有( )
| A.4种 | B.5种 | C.6种 | D.7种 |
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:单选题
下列解释事实的化学方程式或离子方程式,不正确的是
A.工业上可用电解法制备Mg:MgCl2(熔融) Mg + Cl2↑ Mg + Cl2↑ |
| B.向Ca(ClO)2溶液中通入少量CO2:Ca2++2ClO-+H2O+CO2=2HClO+CaCO3↓ |
C.用CaSO4治理盐碱地:CaSO4(s) + Na2CO3(aq) CaCO3(s) + Na2SO4(aq) CaCO3(s) + Na2SO4(aq) |
| D.用FeSO4除去酸性废水中的Cr2O72-:Cr2O72- + Fe2+ + 14H+ ="=" 2Cr3+ + Fe3+ + 7H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某溶液中存在较多的H+、SO42-、NO3-,还可能大量存在的离子组是
| A.Al3+、CO32-、Cl- | B.Na+、NH4+、Cl- |
| C.Mg2+、Cl-、Fe2+ | D.Mg2+、Ba2+、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A.0.1 mol·L-1 NaOH溶液:K+、Ba2+、Cl-、HCO3- |
| B.0.1 mol·L-1 Na2CO3溶液:K+、NH4+、NO3-、SO42- |
| C.0.1 mol·L-1 FeCl3溶液:K+、Na+、I-、SCN- |
| D.0.1 mol·L-1 HCl的溶液:Ca2+、Na+、ClO-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
1L某混合溶液中,溶质X、Y浓度都为0.1mol/L,向混合溶液中滴加某溶液Z(0.1mol/L氢氧化钠或硫酸溶液),所得沉淀的物质的量如图所示,则X、Y、Z分别是
| A.氯化铝、氯化铁、氢氧化钠 | B.氯化铝、氯化镁、氢氧化钠 |
| C.偏铝酸钠、氢氧化钡、硫酸 | D.偏铝酸钠、氯化钡、硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列实验现象所对应的离子方程式不正确的是 ( )。
| 选项 | 实验 | 现象 | 离子方程式 |
| A | 将稀硫酸滴加到KI淀粉溶液中 | 在空气中放置一段时间后溶液呈蓝色 | 4H++4I-+O2=2I2+2H2O |
| B | 用硫氰化钾溶液检验某溶液中含有Fe3+ | 溶液变成红色 | Fe3++3SCN-= Fe(SCN)3 |
| C | 酸性KMnO4溶液中加入Na2SO3溶液 | 溶液紫色褪去 | 2MnO4-+5SO32-+6H+ =2Mn2++5SO42-+3H2O |
| D | 将稀硫酸滴加到含有酚酞的Ba(OH)2溶液中 | 有白色沉淀生成,溶液由红色变成无色 | Ba2++OH-+H++SO42- =BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
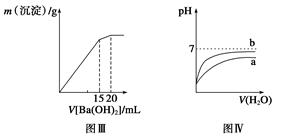
下列图示与对应的叙述相符的是( )
| A.图Ⅰ表示常温下盐酸滴加到0.1 mol·L-1某碱溶液中得到的滴定曲线,由图Ⅰ可知二者恰好中和时,所得溶液的pH>7 |
B.图Ⅱ表示一定条件下进行的反应2SO2+O2 2SO3 ΔH<0各成分的物质的量变化,t2时刻改变的条件可能是升高温度 2SO3 ΔH<0各成分的物质的量变化,t2时刻改变的条件可能是升高温度 |
| C.图Ⅲ表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20 mL Ba(OH)2溶液时,沉淀全部是BaSO4 |
| D.图Ⅳ表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应的是盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各组关于强电解质、弱电解质、非电解质的归类,完全正确的是( )
| | A | B | C | D |
| 强电解质 | Fe | NaCl | CaCO3 | HNO3 |
| 弱电解质 | CH3COOH | NH3 | H3PO4 | Fe(OH)3 |
| 非电解质 | C12H22O11 (蔗糖) | BaSO4 | C2H5OH | H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在含1 mol KAl(SO4)2的溶液中逐滴加入2 mol Ba(OH)2溶液,下列有关说法中正确的是( )
| A.先生成沉淀,后沉淀全部溶解 |
| B.当溶液中Ba2+全部沉淀出来时,沉淀的总物质的量最大 |
| C.最后得到的沉淀是BaSO4 |
| D.最后的沉淀为2 mol BaSO4、1 mol Al(OH)3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com