
分析 (1)碳酸钾与盐酸反应生成气体,而KCl不能;HCl与饱和亚硫酸氢钠溶液反应生成二氧化硫;
(2)碳酸氢钠加热分解生成碳酸钠,碘与四氯化碳互溶,但沸点不同;
(3)SiO2与NaOH溶液反应,而氧化铁不能.
解答 解:(1)碳酸钾与盐酸反应生成气体,而KCl不能,则鉴别试剂为稀盐酸;HCl与饱和亚硫酸氢钠溶液反应生成二氧化硫,则除杂试剂为饱和亚硫酸氢钠溶液,
故答案为:稀盐酸;饱和亚硫酸氢钠溶液;
(2)碳酸氢钠加热分解生成碳酸钠,则除杂方法为加热,碘与四氯化碳互溶,但沸点不同,则分离碘和四氯化碳的方法为蒸馏,故答案为:加热;蒸馏;
(3)SiO2与NaOH溶液反应,而氧化铁不能,则除杂试剂为NaOH溶液,发生的离子反应为SiO2+2OH-=SiO32-+H2O,故答案为:NaOH溶液;SiO2+2OH-=SiO32-+H2O.
点评 本题考查混合物分离提纯及鉴别,为高频考点,把握物质的性质、性质差异、发生的反应及混合物分离方法等为解答的关键,侧重分离提纯试剂选择及方法的考查,注意元素化合物知识的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
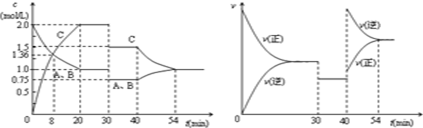
| A. | 30min时降低温度,40min时升高温度 | |
| B. | 8min时反应平衡 | |
| C. | 反应方程式中的x=1,正反应为放热反应 | |
| D. | 该反应20~30min的平衡常数比30~40min的平衡常数大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 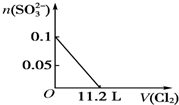 | B. | 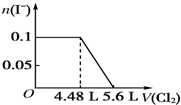 | ||
| C. | 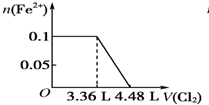 | D. | 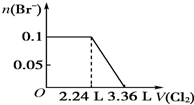 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “物质的量”的单位是g.mol-1 | |
| B. | 22.4LN2所含分子数NA | |
| C. | 0.1mol铁与足量的盐酸反应,失去的电子数为0.3NA | |
| D. | 0.1mol CO2中所含氧原子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaNO3 | B. | Mg(NO3)2 | ||
| C. | AgNO3 | D. | NaNO3和AgNO3的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{m}{a}L$ | B. | $\frac{2m}{3a}L$ | C. | $\frac{m+n}{a}L$ | D. | $\frac{2(m+n)}{3a}L$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuSO4•3H2O | B. | CuSO4•2H2O | C. | CuSO4•H2O | D. | CuSO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com