
| A. | 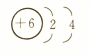 | B. | 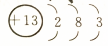 | C. | 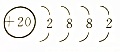 | D. | 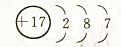 |
科目:高中化学 来源: 题型:解答题
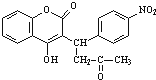
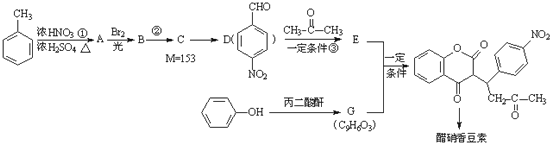
 +H2O
+H2O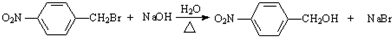 .
.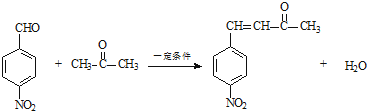 .
.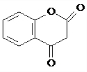 .
.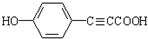 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐析可提纯蛋白质并保持其生理活性 | |
| B. | 油脂碱性或者酸性条件下的水解反应叫做皂化反应 | |
| C. | 打针时用75%的乙醇溶液消毒是蛋白质变性知识的应用 | |
| D. | 蛋白质、纤维素、淀粉都是高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
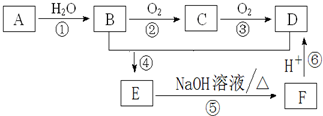 已知:烃 A的摩尔质量为28g/mol,有关A的转化关系如图所示,请回答下列问题:
已知:烃 A的摩尔质量为28g/mol,有关A的转化关系如图所示,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
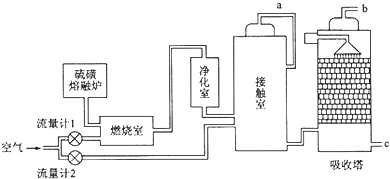
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜锌原电池中铜是正极 | |
| B. | 铁壳船底部镶嵌铜块,铜块更易被腐蚀 | |
| C. | 用电解法精炼粗铜时粗铜作阳极 | |
| D. | 在镀件上镀铜是可用金属铜作阳极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大气中CO2含量的剧增,对自然界中碳及其化合物间的平衡没有影响 | |
| B. | 木炭燃烧过程中,存在碳单质、CO和CO2之间的转化 | |
| C. | 碳的氧化物间的相互转化不属于氧化还原反应 | |
| D. | 含碳的无机化合物和有机化合物之间存在着严格的界限,无机化合物不能合成有机化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com