
| 点燃 |
| Cu |
| △ |
| 浓硫酸 |
| △ |
| 点燃 |
| Cu |
| △ |
| 浓硫酸 |
| △ |


科目:高中化学 来源: 题型:

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Al(OH)3 | Zn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 5.4 | 4.0 | 6.5 |
| 完全沉淀 | 3.7 | 9.6 | 6.4 | 5.2 | 8.0 |
| c(Fe2-) |
| c(Cu2-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | 物质的摩尔质量(g/mol) | 质量 | 0℃密度(g/cm3) | 体积(cm3) |
| Fe | 55.85 | 7.8 | ||
| Al | 26.98 | 2.7 | ||
| H2O | 18 | 1.0 | ||
| H2SO4 | 98 | 1.83 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
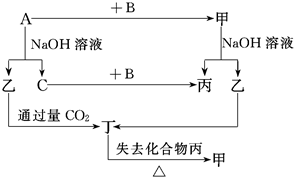
查看答案和解析>>
科目:高中化学 来源: 题型:
 在温度为373K时,将0.100mol无色的N2O4气体通入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O42NO2的平衡.如图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
在温度为373K时,将0.100mol无色的N2O4气体通入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O42NO2的平衡.如图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)| T/K | 323 | 373 |
| K值 | 0.022 | ? |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、核糖和脱氧核糖 |
| B、分子式为C4H6和C5H8的烃 |
| C、葡萄糖和蔗糖 |
| D、分子式为C4H10和C20H42的烃 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com