
| A. | 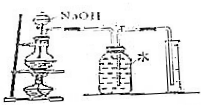 测定氨盐纯度 | B. | 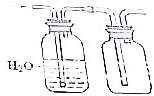 除去NO2并收集NO | ||
| C. | 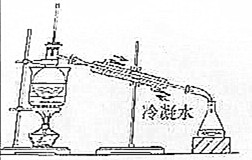 分离四氯化碳和二氯甲烷 | D. | 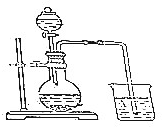 验证中和反应是放热反应 |
分析 A.氨气极易溶于水,不能排水测定氨气的体积;
B.二氧化氮与水反应,NO不能利用排空气法收集;
C.四氯化碳和二氯甲烷互溶,沸点不同,但冷水应下进长出;
D.若放热,烧瓶中气体体积增大,烧杯中有气泡冒出.
解答 解:A.氨气极易溶于水,不能排水测定氨气的体积,则图中装置不能测定铵盐的纯度,故A错误;
B.二氧化氮与水反应生成NO,但NO易被氧化,则不能利用排空气法收集NO,故B错误;
C.四氯化碳和二氯甲烷互溶,沸点不同,但冷水应下进长出,图中冷水的方向不合理,故C错误;
D.若放热,烧瓶中气体体积增大,烧杯中有气泡冒出,则图中装置可验证中和反应是放热反应,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应、实验装置的作用、混合物分离等为解答的关键,侧重分析与实验能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | Na、K都是I A族的金属,Na常温下与水剧烈反应,故K常温下也能与水剧烈反应 | |
| B. | HCl的水溶液是强酸,推出HF的水溶液也是强酸 | |
| C. | 由“2Fe+3Cl2=2FeCl3”反应可推出“2Fe+3I2=2FeI3”反应也能发生 | |
| D. | 由“Cl2+H2O?HCl+HClO”反应可推出“F2+H2O?HF+HFO”反应也能发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 先加入酸性高锰酸钾溶液;加稀硝酸酸化后加银氨溶液,微热 | |
| B. | 先加入溴水;加稀硝酸酸化后加酸性高锰酸钾溶液 | |
| C. | 先加入新制氢氧化铜悬浊液,加热;加稀硝酸酸化,再加入溴水 | |
| D. | 先加入银氨溶液;再另取该物质加入溴水 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
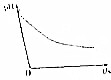 某离子反应涉及H2O、CLO-、NH4+、H+、N2、CL-六种微粒.常温条件下反应时,溶液pH随时间变化的曲线如图所示,下列判断错误的是( )
某离子反应涉及H2O、CLO-、NH4+、H+、N2、CL-六种微粒.常温条件下反应时,溶液pH随时间变化的曲线如图所示,下列判断错误的是( )| A. | 该反应的氧化剂是CLO- | |
| B. | 该反应中有两种离子生成 | |
| C. | 该反应生成1mol氧化产物时,转移的电子为6mol | |
| D. | 参加反应的氧化剂与还原剂的物质的量之比为2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Cl-、HCO3-、Ca2+ | B. | OH-、Na+、Mg2+、HCO3- | ||
| C. | Na+、Cl-、H+、Ag+ | D. | Na+、SiO32-、H+、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com