
| A、①④⑥⑦ | B、①③⑤⑧ |
| C、②③④⑦ | D、①④⑥⑧ |


 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
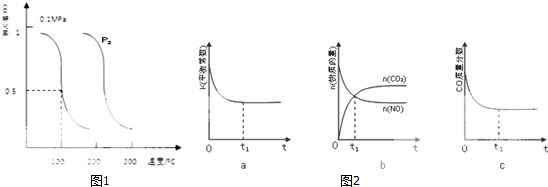
| 容器 | A | B | C |
| 反应物投入量 | 1molCO2(g)和 3molH2(g) | 1molCH3OH(g)和 1molH2O(g) | 2molCO2(g)和6mol H2(g) |
| CH3OH(g)浓度(mol/L) | c1 | c2 | c3 |
| 反应能量变化 | 放出29.4kJ | 吸收a kJ | 放出b kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、葡萄糖可以转变成脂肪,储存在脂肪组织中,过多食用糖类容易使人发胖 |
| B、某些植物油和鱼油中的不饱和甘油酯含量丰富,而动物脂肪中饱和甘油酯含量很高 |
| C、蛋白质溶液遇到浓的硫酸铵、硫酸钠等无机盐溶液,会析出沉淀,这个过程称为变性 |
| D、人体对维生素的需求量很小,但是,人类的生命活动不可缺少它 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、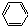 +HO-NO2 +HO-NO2
 +H2O;取代反应 +H2O;取代反应 | |||
| B、CH2=CH2+Br2→CH2Br-CH2Br;加成反应 | |||
C、2CH3CH2OH+O2
| |||
D、CH3COOH+CH3CH2OH
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com