
| A. | 常温下,100 mL 1 mol•L-1 FeCl3溶液中含有Fe3+数目小于0.1NA | |
| B. | 1 mol-OH和17 g NH3所含的电子数相等 | |
| C. | 标准状况下,2.24 L Cl2与过量铁粉反应,转移的电子总数为2NA | |
| D. | 常温下,23 g NO2和N2O4的混合气体中含有NA个氧原子 |
分析 A.依据三价铁离子水溶液中部分水解的性质解答;
B.1个-OH含有9个电子,1个NH3含有10个电子;
C.氯气与铁反应生成氯化铁,氯气不足依据氯气的量计算转移电子数目;
D.NO2和N2O4具有相同的最简式NO2,据此解答.
解答 解:A.三价铁离子为弱碱阳离子,水溶液中部分水解常温下,所以100 mL 1 mol•L-1 FeCl3溶液中含有Fe3+数目小于0.1NA,故A正确;
B.1个-OH含有9个电子,1个NH3含有10个电子,则1 mol-OH含有9mol电子,17 g NH3所含的电子数为10mol,故B错误;
C.标准状况下,2.24 L Cl2物质的量为0.1mol,与过量铁粉反应,氯气不足完全反应,转移的电子总数为2NA,故C正确;
D.23 g NO2和N2O4的混合气体含有NO2原子团物质的量为$\frac{23g}{46g/mol}$=0.5mol,含有O物质的量为0.5mol×2=1mol,含有NA个氧原子,故D正确;
故选:B.
点评 本题考查阿伏加德罗常数的有关计算和判断,侧重考查了学生对物质的量、粒子数、质量、体积等与阿伏加德罗常数关系的理解,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,还要准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,题目难度不大.


科目:高中化学 来源: 题型:解答题
 | NO | N2 | CO2 |
| 0 | 2.00 | 0 | 0 |
| 10 | 1.16 | 0.42 | 0.42 |
| 20 | 0.80 | 0.60 | 0.60 |
| 30 | 0.80 | 0.60 | 0.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3+HCl═NaCl+H2O+CO2↑ | B. | 2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$ 2KCl+2O2↑ | ||
| C. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 | D. | 2CuO+C$\frac{\underline{\;\;△\;\;}}{\;}$2Cu+CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| B. | 常温下,1 L 0.1 mol•L-1的NH4NO3溶液中氮原子数为0.2NA | |
| C. | 10 L pH=1的硫酸溶液中含有的H+为2NA | |
| D. | 欲配制1.00 L 1.00 mol•L-1的NaCl溶液,可将58.5 g NaCl溶于1.00 L水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L 0.1mol/L的氨水中有0.1NA个NH4+ | |
| B. | 标准状况下,22.4L盐酸含有NA个HCI分子 | |
| C. | 常温常压下,14g由N2与CO的混合气体含有0.5NA个原子 | |
| D. | 标准状况下,6.72L N02与水充分反应转移0.2NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
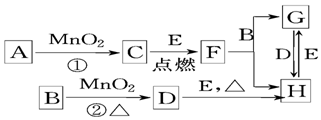
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com