
| A.水、CCl4、酒精、汽油 |
| B.NaCl溶液、NaBr溶液、NaI溶液、NaOH溶液 |
| C.AgNO3溶液、NaOH溶液、KI溶液、CCl4 |
| D.CCl4、酒精、NaCl溶液、KI-淀粉溶液 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
| 序号 | 实验内容 | 实验目的 |
| A | 室温下,使用pH计测定浓度均为0.1mol/L NaClO溶液CH3COONa | 比较HClO和CH3COOH的酸性强弱 |
| B | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,再加入新制银氨溶液,水浴加热 | 检验蔗糖水解产物具有还原性 |
| C | 向新生成的AgCl悬浊液中滴入KI溶液 | 研究沉淀的转化 |
| D | 室温下,向两支装有同体积同浓度过氧化氢溶液的试管中,分别加入3滴同浓度的氯化铜、氯化铁溶液 | 研究催化剂对反应速率的影响 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作、现象 | 实验结论 |
| A | 将FeCl3溶液分别滴入NaBr、NaI溶液中,再分别滴加CCl4,振荡,静置 | 氧化性:Fe3+>Br2>I2 |
| B | 除锈的铁钉在浓硝酸中浸泡后,用蒸馏水洗净,再放入CuSO4溶液中无现象 | 铁钉表面形成了一层致密稳定的氧化膜 |
| C | 向某溶液中加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸沉淀不消失 | 该溶液中有SO42- |
| D | 甲苯中滴入少量浓溴水,振荡,静置,溴水层褪色 | 萃取了浓溴水中的溴 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
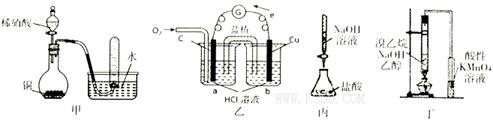
| A.用甲装置验证铜与稀硝酸的反应产物是NO |
B.通过乙装置实现化学反应: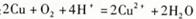 |
| C.用丙装置测定盐酸的浓度 |
| D.用丁装置检验溴乙烷与NaOH醇溶液共热有乙烯生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
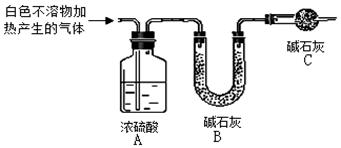
 H+ + OH-、HCO3-
H+ + OH-、HCO3- H+ +CO32-,请从平衡移动角度分析实验①产生大量气体和白色不溶物的原因: 。
H+ +CO32-,请从平衡移动角度分析实验①产生大量气体和白色不溶物的原因: 。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
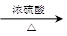 CH3CH2CHCH2↑+H2O
CH3CH2CHCH2↑+H2O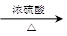 (n?C4H9)2O+H2O
(n?C4H9)2O+H2O| A.减少HBr的挥发 |
| B.防止正丁醇的挥发 |
| C.防止溴化钠被氧化 |
| D.防止温度过高导致炭化结焦 |
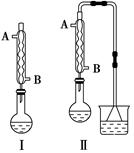
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.证明一瓶红棕色气体是溴蒸气还是二氧化氮,可用湿润的碘化钾淀粉试纸检验,观察试纸颜色的变化 |
| B.铝热剂溶于足量稀盐酸再滴加KSCN溶液,未出现血红色,该铝热剂不含氧化铁 |
| C.测氯水的pH可用玻璃棒蘸取氯水点在pH试纸上,待其变色后和标准比色卡比较 |
| D.用新制氢氧化铜悬浊液可以鉴别甲酸、甲酸甲酯、乙酸、乙酸乙酯四种物质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
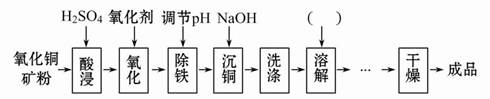

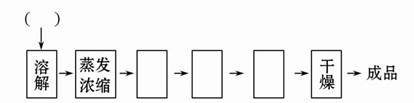
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
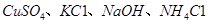 四种成分中的某两种。通过实验确定其组成:取少量固体溶于水,得到无色澄清的溶液;向该溶液滴入少量的硝酸铝溶液,看到有白色沉淀生成。该固体混合物的组成是
四种成分中的某两种。通过实验确定其组成:取少量固体溶于水,得到无色澄清的溶液;向该溶液滴入少量的硝酸铝溶液,看到有白色沉淀生成。该固体混合物的组成是| A.KC1、NaOH | B.KC1、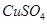 | C.NaOH、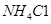 | D.KC1、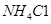 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com