
| 实验步骤 | 实验结论 |
| ①氯水+1mLCCl4,振荡,静置,观察四氯化碳层颜色 | 氧化性从强到弱的顺序:氯、溴、碘 |
| ②NaBr溶液+氯水+1mLCCl4,振荡,静置,观察四氯化碳层颜色 | |
| ③KI溶液+氯水+1mLCCl4,振荡,静置,观察四氯化碳层颜色 |
分析 (1)该实验用量筒量取试剂,可在试管中进行反应;
(2)②中反应的化学方程式为 2NaBr+Cl2=2NaCl+Br2;③中反应的离子方程式为2I-+Cl2=2Cl-+I2;
(3)四氯化碳不参加反应,但卤素单质不易溶于水,易溶于四氯化碳;
(4)不能比较溴、碘的氧化性强弱,以此来解答.
解答 解:由非金属单质间的置换反应来比较单质的氧化性强弱可知,Cl2能置换出Br2、I2,Br2能置换出I2,则说明氧化性Cl2>Br2>I2,
(1)该实验用量筒量取试剂,可在试管中进行反应,还需要胶头滴管滴加液体,故答案为:试管、胶头滴管;
(2)②中反应的化学方程式为 2NaBr+Cl2=2NaCl+Br2;③中反应的离子方程式为2I-+Cl2=2Cl-+I2,故答案为:2NaBr+Cl2=2NaCl+Br2;2I-+Cl2=2Cl-+I2;
(3)四氯化碳不参加反应,但卤素单质不易溶于水,易溶于四氯化碳,所以其作用为萃取剂,使生成的Br2、I2溶于其中,便于观察现象:萃取剂;
(4)设计的实验中不能证明溴的氧化性强于碘,把第③步改为:KI溶液+溴水+1mL CCl4,振荡,静置,观察CCl4层颜色,故答案为:没有比较Br2和I2的氧化性强弱;把第③步改为:将溴水滴在KI淀粉试纸上,观察试纸是否变蓝色(或KI溶液+溴水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色).
点评 本题考查卤素单质之间的置换反应的实验设计,把握单质的氧化性强弱及现象的分析为解答的关键,涉及氧化还原反应氧化性的比较及萃取等知识点,题目难度不大.


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲>乙>丙>丁 | B. | 乙>甲>丙>丁 | C. | 丁>丙>乙>甲 | D. | 乙>甲>丁>丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
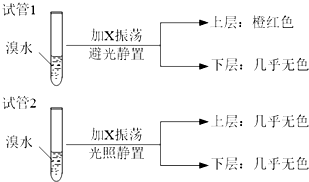
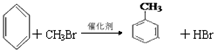 ;②C物质苯环上一卤代物只有两种.
;②C物质苯环上一卤代物只有两种.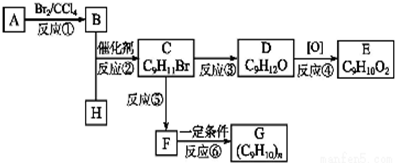
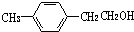 ,F的分子式C9H10.
,F的分子式C9H10.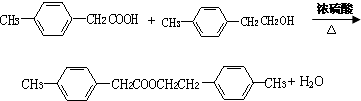 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3和稀盐酸 | B. | Al2O3和水 | C. | Al2(SO4)3和NaOH | D. | AlCl3和氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ;
; .
.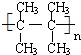 在催化剂作用下,与H2加成后的产物名称为2,3-二甲基丁烷.
在催化剂作用下,与H2加成后的产物名称为2,3-二甲基丁烷.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu$\stackrel{O_{2},CO_{2},H_{2}O}{→}$Cu2(OH)2CO3$\stackrel{△}{→}$Cu(OH)2 | |
| B. | MgO$\stackrel{HCl(aq)}{→}$MgCl2(aq)$\stackrel{加热,HCl氛围}{→}$MgCl2(s) | |
| C. | CaCl2(aq)$\stackrel{CO_{2}}{→}$CaCO3$\stackrel{SiO_{2}/高温}{→}$CaSiO3 | |
| D. | S$\stackrel{O_{2}/点燃}{→}$SO3$\stackrel{H_{2}O}{→}$H2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com