
| A. | Cl2 | B. | SO2 | C. | N2 | D. | NH3 |
科目:高中化学 来源: 题型:选择题
| A. | 开发利用太阳能与风能是发展低碳经济的重要途径 | |
| B. | 地沟油对人体危害严重,查证没收后应燃烧处理 | |
| C. | 氮化硅、碳化硅可做耐高温、耐磨材料 | |
| D. | 氯气、臭氧、高铁酸钾都是常用的自来水消毒剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3对 | B. | 4对 | C. | 5对 | D. | 6对 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
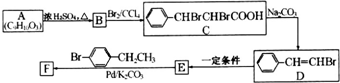
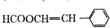 (写结构简式).
(写结构简式).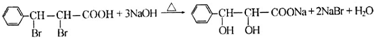
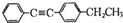 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 易失去电子的物质 | B. | 原子核外有10个电子的微粒 | ||
| C. | 原子的最外层只有1个电子的元素 | D. | 原子核内有12个质子的元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1×10-2 mol•L-1 | B. | 1×10-8 mol•L-1 | C. | 1×10-12 mol•L-1 | D. | 1×10-4 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
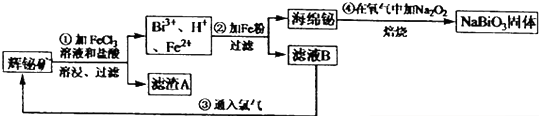
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 | B. | 2.22 | C. | 3.46 | D. | 4.44 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com