
| H | +4 |
| 1 |
| 8 |
| 1 |
| 2 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 (2012?成都模拟)一水硫酸四氨合铜(Ⅱ)([Cu(NH3)4]SO4?H2O]是一种重要的染料及农药中间体.请回答下列相关问题:
(2012?成都模拟)一水硫酸四氨合铜(Ⅱ)([Cu(NH3)4]SO4?H2O]是一种重要的染料及农药中间体.请回答下列相关问题:| H | + 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
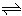 Cu2++4NH3
Cu2++4NH3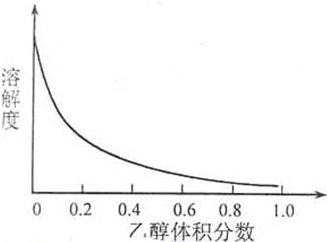
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源:2012届河北省石家庄市高三第二次模拟理科综合化学试卷(带解析) 题型:填空题
[化学一选修3:物质结构与性质](15分)
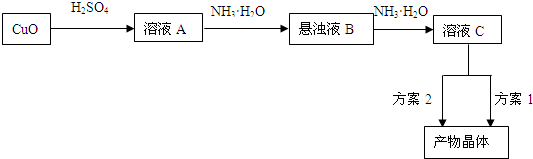
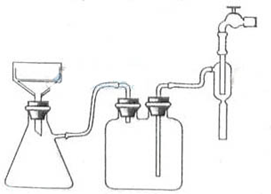
一水硫酸四氨合铜(II)(化学式为 是一种重要的染料及农药中间体。某学习小组以孔雀石(主要成分为Cu2(OH)2CO3,含少量Fe2O3和SO2杂质)为原料制备该物质的流程如下:
是一种重要的染料及农药中间体。某学习小组以孔雀石(主要成分为Cu2(OH)2CO3,含少量Fe2O3和SO2杂质)为原料制备该物质的流程如下:
请回答:
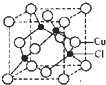
(1) 沉淀A的晶体中最小环上的原子个数为______,气体C分子中 键和
键和 键的个数比为______
键的个数比为______
(2) 溶液D的溶质阴离子的空间构型为______,其中心原子的杂化轨道类型为______
(3) MgO的熔点高于CuO的原因为____________
(4) 画出一水硫酸四氨合铜(II)中配离子 的配位键____________。
的配位键____________。
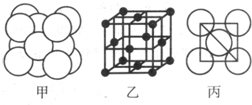
(5)湿法炼铜就是利用溶液D制得铜单质,铜单质晶体中原子的堆积方式如图甲所示,其晶胞如图乙所示,原子之间相互位置关系的平面图如图丙所示。
①铜单质晶体中原子的堆积方式为____________,晶胞中Cu原子的配位数为______
②若Cu原子半径为acm,则Cu单质晶体的密度为______g/cm3(只列出计算式,阿伏加德罗常数的值为NA)。
查看答案和解析>>
科目:高中化学 来源:2014届湖北省高二下学期期中考试化学试卷(解析版) 题型:实验题
一水硫酸四氨合铜(Ⅱ)(化学式为[Cu(NH3)4]SO4·H2O)是一种重要的染料及农药中间体。某学习小组以孔雀石(主要成分为Cu2(OH)2CO3,含少量Fe2O3和SiO2杂质)为原料制备该物质的流程如下:

请回答:
(1)沉淀A的晶体中最小环上的原子个数为________,气体C分子中σ键和π键的个数比为________。
(2)溶液D的溶质阴离子的空间构型为__________,其中心原子的杂化轨道类型为________。
(3)MgO的熔点高于CuO的原因为______________________________________。
(4)画出一水硫酸四氨合铜(Ⅱ)中配离子([Cu(NH3)4]2+)的配位键________________。
(5)一种铜金合金晶体具有面心立方最密堆积的结构。在晶胞中,Au原子位于顶点,Cu原子位于面心,则该合金中Au原子与Cu原子个数之比为 ,若该晶胞的边长为a pm,则合金的密度为 g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com