
(16分)酯交换法广泛应用于医药、生物制剂等有机合成路线,下列反应①②均为酯交换反应。
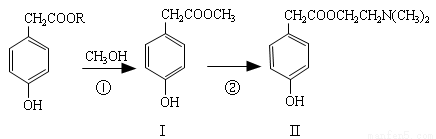
(1)化合物I的分子式是_______________,1mol化合物I完全燃烧,消耗_____mol氧气。
(2)酯交换属于 _反应(填“取代、加成、消去”)。写出物质I在稀硫酸或氢氧化钠条件下水解的化学反应方程式:_______________。
(3)下列关于化合物I的说法正确的是_________。
A.化合物I可与浓溴水反应生成白色沉淀
B.1mol化合物I最多能与2mol氢氧化钠发生反应
C.化合物I可以发生银镜反应
D.化合物I的核磁共振氢谱有五个峰
(4)化合物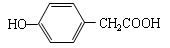 有多种同分异构体,写出符合下列要求的同分异构体___________________________。
有多种同分异构体,写出符合下列要求的同分异构体___________________________。
a.能与FeCl3发生显色反应;
b.苯环上的一氯代物有两种;
c.能与氢氧化钠发生水解反应。
(1)C9H10O3 (2分) 10(2分)
(2)取代(2分)
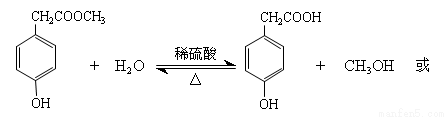
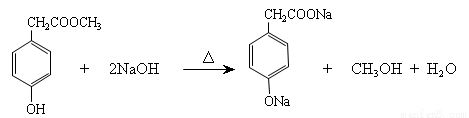 (3分)
(3分)
(3)ABD(3分)(选对一项得一分,选错一项倒扣一分)
(4)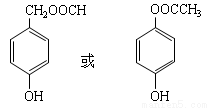 (4分)
(4分)
【解析】
试题分析:(1)化合物I的结构简式也可以表示为:HO—C6H4—CH2COOCH3,故分子式为:C9H10O3,根据有机物燃烧反应方程式:CxHyOz+(x+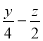 )O2
)O2 xCO2+
xCO2+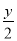 H2O可知,1mol化合物I完全燃烧,消耗
H2O可知,1mol化合物I完全燃烧,消耗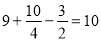 mol氧气;
mol氧气;
(2)酯交换是将两反应物的烃基互换属于取代反应,I在稀硫酸条件下水解生成甲醇与对羟其苯甲酸,在氢氧化钠溶液中水解产生的对羟其苯甲酸会与NaOH继续反应,故反应的方程式分别为:


(3)化合物I含有酯基和酚羟基,可与浓溴水发生取代反应生成白色沉淀;由(2)小题中反应方程式中可以看到1mol化合物I最多能与2mol氢氧化钠发生反应;化合物I中不含醛基,不能发生银镜反应;化合物I分子中国五种不同环境的氢原子,其核磁共振氢谱有五个峰。
(4)满足化合物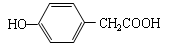 的同分异构体,能与FeCl3发生显色反应的物质必须含有酚羟基,则其他碳原子只能在另一个侧链上,即苯环上有两个取代基,且苯环上的一氯代物有两种,则必须是对位,能与氢氧化钠发生水解反应必须属于酯类物质,综上,符合条件的只有
的同分异构体,能与FeCl3发生显色反应的物质必须含有酚羟基,则其他碳原子只能在另一个侧链上,即苯环上有两个取代基,且苯环上的一氯代物有两种,则必须是对位,能与氢氧化钠发生水解反应必须属于酯类物质,综上,符合条件的只有 。
。
考点:考查钠的物理性质、化学性质及保存以及钠的氧化物的化学性质。


 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案科目:高中化学 来源:2015届广东省湛江市高三第一次月考理综化学试卷(解析版) 题型:选择题
下列实验操作、现象和解释都正确的是
选项 | 实验操作 | 现象 | 解释 |
A. | 向某溶液中加入盐酸 | 产生无色气体 | 溶液中一定含有CO32? |
B. | 新制Fe(OH)2露置于空气中一段时间 | 白色固体迅速变为灰绿色,最终变为红褐色 | 说明Fe(OH)2易被氧化成Fe(OH)3 |
C. | 在CuSO4溶液中加入KI溶液,再加入苯,振荡 | 上层呈紫红色,下层有白色沉淀生产 | 铜离子可以氧化碘离子,白色沉淀可能为CuI |
D. | 向某无色溶液中滴加硝酸酸化的BaCl2溶液 | 产生白色沉淀 | 溶液中一定含有SO42- |
查看答案和解析>>
科目:高中化学 来源:2015届广东省惠州市高三第二次调研考试化学试卷(解析版) 题型:选择题
下列装置、试剂选用或操作正确的是
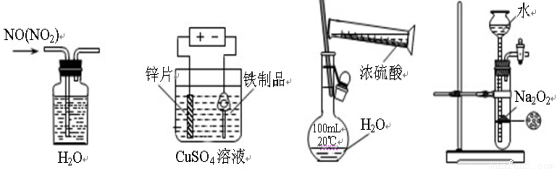
A.除去NO中的NO2 B.铁制品表面镀锌 C.稀释浓硫酸 D.制备少量O2
查看答案和解析>>
科目:高中化学 来源:2015届广东省广州市高三上学期期中考试理综化学试卷(解析版) 题型:填空题
(16分)目前世界上已证明“达菲”是治疗禽流感和甲型H1N1流感的良方。“达菲”的主要合成原料是我国盛产的莽草酸。从八角茴香中提取的莽草酸经过多次反应和其他工艺制成“达菲”颗粒。下图是莽草酸和“达菲”有效成分的键线式结构(楔形实线、虚线表示基团的立体结构)。
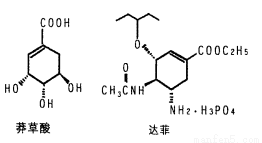
(1)“达菲”的相对分子质量为410.4,扣除H3PO4后的部分称为“自由基奥司他韦”。试求“自由基奥司他韦”的相对分子质量________;“自由基奥司他韦”能与磷酸结合,说明氨基具有________性。
(2)莽草酸中含有的官能团有__________________________(写名称)。
(3)下列有关莽草酸的说法中正确的是____________________________。
①分子式为C7H10O5
②能使FeCl3溶液显紫色
③能使溴的四氯化碳溶液褪色
④l mol莽草酸与分别足量的Na和NaOH反应,消耗的Na和NaOH的物质的量之比为4:l
(4)莽草酸与C2H5OH发生酯化反应的化学方程式是_________________。
(5)莽草酸在浓硫酸作用下加热可得到B(C7H6O3),B的同分异构体中既含有酚羟基又含有酯基的共有______种,写出其中一种同分异构体的结构简式 。
查看答案和解析>>
科目:高中化学 来源:2015届广东省广州市高三上学期期中考试理综化学试卷(解析版) 题型:选择题
NA表示阿伏伽德罗常数,下列判断正确的是
A.在20 g D216O中含有10NA个电子
B.标准状况下,2.24 L己烷所含分子数为0.1NA
C.1 mol Cl2参加反应转移电子数一定为2NA
D.含NA个Na+的Na2O溶解于1 L水中,Na+的物质的量浓度为1 mol/L
查看答案和解析>>
科目:高中化学 来源:2015届广东省增城市毕业班调研测试理科综合化学试卷(解析版) 题型:选择题
设nA为阿伏加德罗常数的数值,下列说法正确的是
A.常温常压下,16 g O2含有nA个氧原子
B.1mol苯含有3nA个碳碳单键和3nA个碳碳双键
C.一定条件下,3molH2和1molN2充分反应后,可得到2nA个NH3分子数
D.1 mol·L-1 FeCl3溶液中含有Cl-总数为3nA
查看答案和解析>>
科目:高中化学 来源:2015届广东省佛山市高三10月月考化学试卷(解析版) 题型:填空题
(16分)对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:
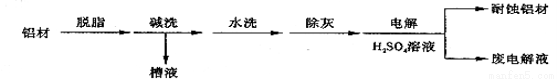
①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时候常有气泡冒出,原因是 (用离子方程式表示)。为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的 。
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,电解后取少量废电解液,加入NaHCO3,溶液后产生气泡和白色沉淀,产生沉淀的原因是 (用离子方程式表示)
(2)镀铜可防止铁制品腐蚀,电镀时用 来做阳极。
(3)利用如图装置,可以模拟铁的电化学防护。

若X为碳棒,为减缓铁的腐蚀,开关K应放于 处,写出X极的电极反应
若X为碳棒,开关K置于M处,写出X极的电极反应
查看答案和解析>>
科目:高中化学 来源:2015届广东省佛山市高三9月考化学试卷(解析版) 题型:选择题
化学知识在生活中有重要意义,下列说法正确的是
A.在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质
B.乙醇、乙酸和甲醛广泛应用于食品加工
C.计算机芯片所用的材料是高纯度的二氧化硅
D.捕获工业排放的CO2能降低地球的温室效应
查看答案和解析>>
科目:高中化学 来源:2015届广东省中山市等五校联考高三第一学期化学试卷(解析版) 题型:实验题
(14分)用霞石岩(化学式为 KNa3[AlSiO4]4 ,主要成份Na2O、K2O、Al2O3、SiO2)制碳酸钠、碳酸钾和氧化铝的工艺流程如下:

已知:①NaHCO3溶液的pH约为8~9,Na2CO3溶液的pH约为11~12。
②溶解过滤工序产生的滤液中含钠、钾和铝的可溶性盐类,钙和硅等其他杂质在滤渣霞石泥中。部分物质的溶解度见下图。

试回答下列问题:
(1)灼烧得到固体M的化学方程式是_______________。
(2)X物质是___________,滤液W中主要含有的离子有____________。(写三种)
(3)操作Ⅰ得到碳酸钠晶体的操作为 、 、 、洗涤、干燥。
(4)碳酸化Ⅰ中发生主要反应的离子方程式是_______________________________。
(5)碳酸化Ⅱ调整pH=8的目的是________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com