
(1)将BaCl2溶液加入样品溶解液中时,怎样判断沉淀是否沉淀完全?
(2)过滤后,为何要用蒸馏水洗涤沉淀?若不洗涤,对实验结果有何影响?
(3)如何判断沉淀是否已洗涤干净?
(4)若称取样品为
解析:该题是混合物组成测定的定量实验,涉及溶解、过滤、洗涤、烘干等基本操作,对于混合物的成分,利用所学知识![]() +Ba2+
+Ba2+![]() BaSO4↓进行定量分析、计算结果。
BaSO4↓进行定量分析、计算结果。
答案:(1)加BaCl2溶液后静置,然后向上层澄清液中再加入BaCl2溶液,如果无沉淀出现,则说明上述沉淀完全;如果有沉淀出现,则还需要再加入BaCl2溶液至不再出现沉淀为止。
(2)过滤后的沉淀上附着有KCl、NaCl和BaCl2,为了保证实验的准确性,必须对沉淀进行洗涤;若不洗涤,测得结果会偏高。
(3)取最后一次洗涤液,滴加AgNO3溶液,若无沉淀出现说明已洗涤干净。
![]()
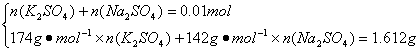
求得n(K2SO4)=0.006 mol
n(Na2SO4)=0.004 mol
![]()
w(Na2SO4)=1-64.8%=35.2%


科目:高中化学 来源: 题型:
| 50w |
| 9av |
| 50w |
| 9av |
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:022
①溶解②加BaCl2溶液 ③过滤 ④洗涤沉淀 ⑤烘干⑥称量等,最后计算结果。问:
(1)将BaCl2溶液加入样品溶解液中时,怎样判断沉淀是否沉淀完全?
(2)过滤后,为何要用蒸馏水洗涤沉淀?若不洗涤,对实验结果有何影响?
(3)如何判断沉淀是否已洗涤干净?
(4)若称取样品为1.612g,最后称得沉淀为2.33g,计算K2SO4和Na2SO4的质量分数。
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
①溶解 ②加BaCl2溶液 ③过滤 ④洗涤沉淀 ⑤烘干 ⑥称量等,最后计算结果。
问:
(1)将BaCl2溶液加入样品溶液中时,怎样判断沉淀是否完全?
(2)过滤后,为何要用蒸馏水洗涤沉淀?若不洗,对实验结果有何影响?
(3)如何判断沉淀已经洗净?
(4)若取样品为1.612g,最后称得沉淀为2.33g,计算K2SO4和Na2SO4的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:058
为了测定K2SO4和NaSO4混合物中各组分的质量分数,分析人员称取该混合物样品Ag并经过如下操作:
①溶解 ②加BaCl2溶液 ③过滤 ④洗涤沉淀 ⑤烘干 ⑥称量等,最后计算结果。
问:
(1)将BaCl2溶液加入样品溶液中时,怎样判断沉淀是否完全?
(2)过滤后,为何要用蒸馏水洗涤沉淀?若不洗,对实验结果有何影响?
(3)如何判断沉淀已经洗净?
(4)若取样品为1.612g,最后称得沉淀为2.33g,计算K2SO4和Na2SO4的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com