
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:阅读理解

| ||
| ||
 则以下叙述正确的是
则以下叙述正确的是查看答案和解析>>
科目:高中化学 来源: 题型:
A、氯碱厂电解饱和食盐水溶液制取NaOH,为了有效地除去粗盐水中Ca2+、Mg2+、
| ||
| B、在接触法制硫酸的工业生产中,SO2氧化为SO3时需要使用催化剂,这样可以提高SO2的转化率 | ||
| C、以石灰石、纯碱、石英为原料,在玻璃窑中加强热制取普通玻璃 | ||
| D、合成氨生产过程中将NH3液化分离,可增大正反应速率,提高N2、H2的转化率 |
查看答案和解析>>
科目:高中化学 来源:2010年广东省高三10月月考化学试题 题型:选择题
下列有关化工生产的说法正确的是
A.将氯气通入澄清石灰水制取漂白粉
B.电解饱和食盐水溶液制取金属钠
C.SO2氧化为SO3时需要使用催化剂,这样可以提高SO2的转化率
D.用98.3%的浓H2SO4吸收SO3,目的是防止形成酸雾,使SO3吸收完全
查看答案和解析>>
科目:高中化学 来源:2010年上海市高一上学期期中考试化学试卷 题型:填空题
氯碱厂电解饱和食盐水溶液制取NaOH的工艺流程示意图如下:
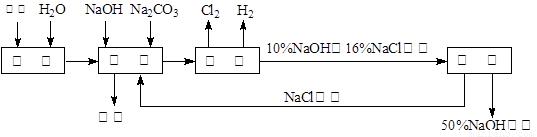
依据上图,完成下列填空:
(1)在电解过程中化学反应方程式为 ,与电源负极相连的电极附近收集到的气体是 。
(2)如果粗盐中SO42—含量较高,必须添加钡试剂除去SO42—,该钡试剂可以是 。
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2 D.BaSO4
(3)如何除去粗盐中含有的CaCl2、MgCl2及Na2SO4(实际上是指Ca2+、Mg2+及 SO42-),具体操作有: A、过滤 B、加足量的BaCl2溶液 C、加适量的稀盐酸
D、加足量的NaOH溶液 E、加足量的Na2CO3溶液
具体操作的顺序为
(4)脱盐工序中,通过加热浓缩、冷却、过滤的方法除去NaCl,该方法利用的是NaOH与NaCl这两物质在 上的性质差异。
(5)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2和NaOH反应;若采用无隔膜电解冷的食盐水,Cl2和NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com