
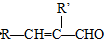 +H2O
+H2O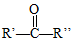 ”ś
”ś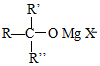 $\stackrel{H+/H_{2}O}{”ś}$
$\stackrel{H+/H_{2}O}{”ś}$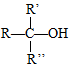

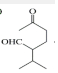 $\stackrel{O{H}^{-}}{”ś}$
$\stackrel{O{H}^{-}}{”ś}$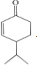 +H2O£®
+H2O£®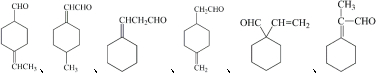
·ÖĪö CµÄ½į¹¹¼ņŹ½ĪŖ £¬øł¾ŻŅŃÖŖĢõ¼žČ©Ź§Č„OH-µĆ£¬DµÄ½į¹¹¼ņŹ½ĪŖ
£¬øł¾ŻŅŃÖŖĢõ¼žČ©Ź§Č„OH-µĆ£¬DµÄ½į¹¹¼ņŹ½ĪŖ £¬øł¾ŻŅŃÖŖĢõ¼žEŗĶ
£¬øł¾ŻŅŃÖŖĢõ¼žEŗĶ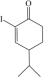 ŌŚH+/H2OµÄ×÷ÓĆĻĀÉś³É
ŌŚH+/H2OµÄ×÷ÓĆĻĀÉś³É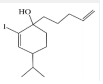 £¬¹ŹEµÄ½į¹¹¼ņŹ½ĪŖCH2=CHCH2CH2CH2MgX£¬¾Ż“Ė½ųŠŠ·ÖĪö£¬
£¬¹ŹEµÄ½į¹¹¼ņŹ½ĪŖCH2=CHCH2CH2CH2MgX£¬¾Ż“Ė½ųŠŠ·ÖĪö£¬
£Ø8£©CH3CH2OHŗĶO2ŌŚCu×÷“߻ƼĮ¼ÓČȵÄĢõ¼žĻĀÉś³ÉCH3CHO£¬CH3CHOŗĶCH3COCH3ĶŃČ„OH-Éś³É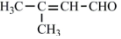 £¬
£¬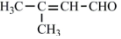 ŗĶH2·¢Éś¼Ó³É·“Ӧɜ³É
ŗĶH2·¢Éś¼Ó³É·“Ӧɜ³É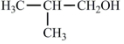 £¬
£¬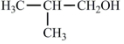 ŗĶO2ŌŚCu×÷“߻ƼĮ¼ÓČȵÄĢõ¼žĻĀÉś³ÉÄæ±ź²śĪļ
ŗĶO2ŌŚCu×÷“߻ƼĮ¼ÓČȵÄĢõ¼žĻĀÉś³ÉÄæ±ź²śĪļ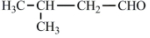 £¬¾Ż“Ė½ųŠŠ·ÖĪö£®
£¬¾Ż“Ė½ųŠŠ·ÖĪö£®
½ā“š ½ā£ŗCµÄ½į¹¹¼ņŹ½ĪŖ £¬øł¾ŻŅŃÖŖĢõ¼žČ©Ź§Č„OH-µĆ£¬DµÄ½į¹¹¼ņŹ½ĪŖ
£¬øł¾ŻŅŃÖŖĢõ¼žČ©Ź§Č„OH-µĆ£¬DµÄ½į¹¹¼ņŹ½ĪŖ £¬øł¾ŻŅŃÖŖĢõ¼žEŗĶ
£¬øł¾ŻŅŃÖŖĢõ¼žEŗĶ ŌŚH+/H2OµÄ×÷ÓĆĻĀÉś³É
ŌŚH+/H2OµÄ×÷ÓĆĻĀÉś³É £¬¹ŹEµÄ½į¹¹¼ņŹ½ĪŖCH2=CHCH2CH2CH2MgX£¬
£¬¹ŹEµÄ½į¹¹¼ņŹ½ĪŖCH2=CHCH2CH2CH2MgX£¬
£Ø1£©øł¾ŻAµÄ½į¹¹¼ņŹ½£¬ŌņAÖŠµÄ¹ŁÄÜĶÅĆū³ĘŹĒōŹ»łŗĶĢ¼Ģ¼Ė«¼ü£¬
¹Ź“š°øĪŖ£ŗĢ¼Ģ¼Ė«¼ü£»
£Ø2£©CµÄ½į¹¹¼ņŹ½ĪŖ £¬DµÄ½į¹¹¼ņŹ½ĪŖ
£¬DµÄ½į¹¹¼ņŹ½ĪŖ £¬Ōņ·“Ó¦¢ŚµÄ»Æѧ·½³ĢŹ½ŹĒ
£¬Ōņ·“Ó¦¢ŚµÄ»Æѧ·½³ĢŹ½ŹĒ $\stackrel{O{H}^{-}}{”ś}$
$\stackrel{O{H}^{-}}{”ś}$ +H2O£¬
+H2O£¬
¹Ź“š°øĪŖ£ŗ $\stackrel{O{H}^{-}}{”ś}$
$\stackrel{O{H}^{-}}{”ś}$ +H2O£»
+H2O£»
£Ø3£©ÓÉŅŌÉĻ·ÖĪöµĆ£¬·“Ó¦¢ŪÖŠŹŌ¼ĮEµÄ½į¹¹¼ņŹ½ŹĒCH2=CHCH2CH2CH2MgX£¬
¹Ź“š°øĪŖ£ŗCH2=CHCH2CH2CH2MgX£»
£Ø4£©·“Ó¦¢Ü·¢Éś·Ö×ÓÄŚĻūČ„·“Ó¦£¬¹Ź»Æѧ·½³ĢŹ½ĪŖ ”ś
”ś +HI£¬¹Ź·“Ó¦¢ÜµÄĮķŅ»ÖÖ²śĪļŹĒHI£¬
+HI£¬¹Ź·“Ó¦¢ÜµÄĮķŅ»ÖÖ²śĪļŹĒHI£¬
¹Ź“š°øĪŖ£ŗHI£»
£Ø5£©øł¾ŻŅŃÖŖĢõ¼žµĆ£¬ŌŚR2CuLiµÄ×÷ÓĆĻĀ·¢Éś¼Ó³É·“Ó¦£¬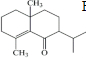 ±Č
±Č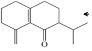 ¶ąĮĖŅ»øö-CH3£¬¹ŹFµÄ½į¹¹¼ņŹ½ŹĒ£ØCH3£©2CuLi£¬
¶ąĮĖŅ»øö-CH3£¬¹ŹFµÄ½į¹¹¼ņŹ½ŹĒ£ØCH3£©2CuLi£¬
¹Ź“š°øĪŖ£ŗ£ØCH3£©2CuLi£»
£Ø6£©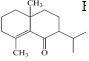 ±Č
±Č ÉŁĮĖ2øöHŌ×Ó£¬¹Ź
ÉŁĮĖ2øöHŌ×Ó£¬¹Ź µ½
µ½ ·¢Éś¼Ó³É·“Ó¦£¬¹ŹFĪŖH2£¬Ęäµē×ÓŹ½ĪŖH£ŗH£¬
·¢Éś¼Ó³É·“Ó¦£¬¹ŹFĪŖH2£¬Ęäµē×ÓŹ½ĪŖH£ŗH£¬
¹Ź“š°øĪŖ£ŗH£ŗH£»
£Ø7£©DµÄ½į¹¹¼ņŹ½ÄÜ·¢ÉśŅų¾µ·“Ó¦¹ŹÓŠČ©»ł£¬ĒŅĀś×ć½į¹¹ĪŖĮłŌŖ»·×“£¬»·ÉĻÓŠ3ÖÖĒāŌ×Ó£¬¹ŹĀś×ćĻĀĮŠĢõ¼žµÄ½į¹¹¼ņŹ½ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ6£» £»
£»
£Ø8£©CH3CH2OHŗĶO2ŌŚCu×÷“߻ƼĮ¼ÓČȵÄĢõ¼žĻĀÉś³ÉCH3CHO£¬CH3CHOŗĶCH3COCH3ĶŃČ„OH-Éś³É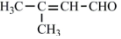 £¬
£¬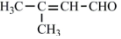 ŗĶH2·¢Éś¼Ó³É·“Ӧɜ³É
ŗĶH2·¢Éś¼Ó³É·“Ӧɜ³É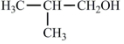 £¬
£¬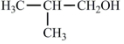 ŗĶO2ŌŚCu×÷“߻ƼĮ¼ÓČȵÄĢõ¼žĻĀÉś³ÉÄæ±ź²śĪļ
ŗĶO2ŌŚCu×÷“߻ƼĮ¼ÓČȵÄĢõ¼žĻĀÉś³ÉÄæ±ź²śĪļ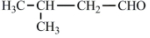 £¬¹ŹŅŌCH3CH2OHÓėCH3COCH3ĪŖŌĮĻ£¬ŗĻ³ÉBµÄĀ·ĻßĪŖCH3CH2OH$\underset{\stackrel{{O}_{2}/Cu}{”ś}}{”÷}$”÷CH3CHO$\underset{\stackrel{C{H}_{3}COC{H}_{3}}{”ś}}{O{H}^{-}}$
£¬¹ŹŅŌCH3CH2OHÓėCH3COCH3ĪŖŌĮĻ£¬ŗĻ³ÉBµÄĀ·ĻßĪŖCH3CH2OH$\underset{\stackrel{{O}_{2}/Cu}{”ś}}{”÷}$”÷CH3CHO$\underset{\stackrel{C{H}_{3}COC{H}_{3}}{”ś}}{O{H}^{-}}$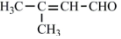 $\stackrel{{H}_{2}}{”ś}$
$\stackrel{{H}_{2}}{”ś}$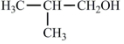 $\underset{\stackrel{{O}_{2}/Cu}{”ś}}{”÷}$
$\underset{\stackrel{{O}_{2}/Cu}{”ś}}{”÷}$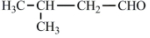 £¬
£¬
¹Ź“š°øĪŖ£ŗCH3CH2OH$\underset{\stackrel{{O}_{2}/Cu}{”ś}}{”÷}$”÷CH3CHO$\underset{\stackrel{C{H}_{3}COC{H}_{3}}{”ś}}{O{H}^{-}}$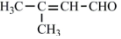 $\stackrel{{H}_{2}}{”ś}$
$\stackrel{{H}_{2}}{”ś}$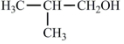 $\underset{\stackrel{{O}_{2}/Cu}{”ś}}{”÷}$
$\underset{\stackrel{{O}_{2}/Cu}{”ś}}{”÷}$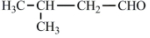 £®
£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļµÄĶʶĻÓėŗĻ³É£¬³ä·ÖĄūÓĆÓŠ»śĪļµÄ·Ö×ÓŹ½Óė½į¹¹½ųŠŠ·ÖĪö½ā“š£¬ŠčŅŖѧɜŹģĮ·ÕĘĪÕ¹ŁÄÜĶŵĊŌÖŹÓė×Ŗ»Æ£¬²ąÖŲæ¼²éѧɜ·ÖĪöĶĘĄķÄÜĮ¦”¢×ŌѧÄÜĮ¦ÓėÖŖŹ¶ĒØŅĘÓ¦ÓĆ£¬ÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
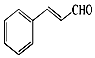 ×ŌČ»½ēÖŠµÄŠķ¶ąÖ²ĪļÖŠŗ¬ÓŠČ©£¬ĘäÖŠÓŠŠ©¾ßÓŠĢŲŹāµÄĻćĪ¶£¬æÉ×÷ĪŖÖ²ĪļĻćĮĻŹ¹ÓĆ£®¹šĘ¤ÖŠŗ¬ÓŠČā¹šČ©£¬½į¹¹ČēĶ¼£¬ŠÓČŹÖŠŗ¬ÓŠ±½¼×Č©£®ŅŌĻĀĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©
×ŌČ»½ēÖŠµÄŠķ¶ąÖ²ĪļÖŠŗ¬ÓŠČ©£¬ĘäÖŠÓŠŠ©¾ßÓŠĢŲŹāµÄĻćĪ¶£¬æÉ×÷ĪŖÖ²ĪļĻćĮĻŹ¹ÓĆ£®¹šĘ¤ÖŠŗ¬ÓŠČā¹šČ©£¬½į¹¹ČēĶ¼£¬ŠÓČŹÖŠŗ¬ÓŠ±½¼×Č©£®ŅŌĻĀĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©| A£® | Čā¹šČ©·Ö×ÓÖŠŗ¬ÓŠĮ½ÖÖ¹ŁÄÜĶÅ£¬·Ö×ÓŹ½ĪŖC9H8O | |
| B£® | Čā¹šČ©·Ö×ÓÖŠ×ī¶ąÓŠ18øöŌ×Ó¹²Ę½Ćę | |
| C£® | 1 molČā¹šČ©ÓėĒāĘų¼Ó³ÉŹ±×ī¶ąĻūŗÄ4 mol H2 | |
| D£® | Čā¹šČ©Óė±½¼×Č©²»ŹĒĶ¬ĻµĪļ£¬µ«¶¼ÄÜ·¢ÉśŃõ»Æ·“Ó¦ŗĶ»¹Ō·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
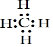 £» BÓėD×é³ÉµÄČżŌ×Ó·Ö×ӵĽį¹¹Ź½ĪŖO=C=O£®
£» BÓėD×é³ÉµÄČżŌ×Ó·Ö×ӵĽį¹¹Ź½ĪŖO=C=O£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1L0.1mol•L-1NH4ClČÜŅŗÖŠ£¬NH4+µÄŹżĮæĪŖ0.1NA | |
| B£® | 2.4gMgÓėH2SO4ĶźČ«·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ0.1NA | |
| C£® | ±ź×¼×“æöĻĀ£¬2.24LN2ŗĶO2µÄ»ģŗĻĘųĢåÖŠ·Ö×ÓŹżĪŖ0.2NA | |
| D£® | 0.1mol H2ŗĶ0.1mol I2ÓŚĆܱÕČŻĘ÷ÖŠ³ä·Ö·“Ó¦ŗó£¬Ęä·Ö×Ó×ÜŹżĪŖ0.2NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ÄæµÄ | ²Ł×÷ | |
| A£® | Č”20.00 mLŃĪĖį | ŌŚ50 mLĖįŹ½µĪ¶Ø¹Ü֊װČėŃĪĖį£¬µ÷Õū³õŹ¼¶ĮŹżĪŖ30.00mLŗ󣬽«Ź£ÓąŃĪĖį·ÅČė׶ŠĪĘæ |
| B£® | ĒåĻ“µāÉż»ŖŹµŃéĖłÓĆŹŌ¹Ü | ĻČÓĆ¾Ę¾«ĒåĻ“£¬ŌŁÓĆĖ®ĒåĻ“ |
| C£® | ²ā¶Ø“×ĖįÄĘČÜŅŗpH | ÓĆ²£Į§°ōÕŗČ”ČÜŅŗ£¬µćŌŚŹŖČóµÄpHŹŌÖ½ÉĻ |
| D£® | ÅäÖĘÅضČĪŖ0.010 mol•LµÄKMnO4ČÜŅŗ | ³ĘČ”KMnO4¹ĢĢå0.158 g£¬·ÅČė100 mLČŻĮæĘæÖŠ£¬¼ÓĖ®Čܽā²¢Ļ”ŹĶÖĮæĢ¶Č |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÄįĮśÉž | B£® | ŠūÖ½ | C£® | ŃņČŽÉĄ | D£® | ĆŽ³ÄŅĀ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
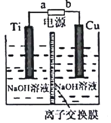
 Č«¹ĢĢ¬ļ®Įņµē³ŲÄÜĮæĆܶČøß”¢³É±¾µĶ£¬Ę乤×÷ŌĄķČēĶ¼ĖłŹ¾£¬ĘäÖŠµē¼«a³£ÓĆ²ōÓŠŹÆÄ«Ļ©µÄS8²ÄĮĻ£¬µē³Ų·“Ó¦ĪŖ£ŗ16Li+xS8=8Li2Sx£Ø2”Üx”Ü8£©£®ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©
Č«¹ĢĢ¬ļ®Įņµē³ŲÄÜĮæĆܶČøß”¢³É±¾µĶ£¬Ę乤×÷ŌĄķČēĶ¼ĖłŹ¾£¬ĘäÖŠµē¼«a³£ÓĆ²ōÓŠŹÆÄ«Ļ©µÄS8²ÄĮĻ£¬µē³Ų·“Ó¦ĪŖ£ŗ16Li+xS8=8Li2Sx£Ø2”Üx”Ü8£©£®ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©| A£® | µē³Ų¹¤×÷Ź±£¬Õż¼«æÉ·¢Éś·“Ó¦£ŗ2Li2S6+2Li++2e-=3Li2S4 | |
| B£® | µē³Ų¹¤×÷Ź±£¬ĶāµēĀ·ÖŠĮ÷¹ż0.02 molµē×Ó£¬øŗ¼«²ÄĮĻ¼õÖŲ0.14 g | |
| C£® | ŹÆÄ«Ļ©µÄ×÷ÓĆÖ÷ŅŖŹĒĢįøßµē¼«aµÄµ¼µēŠŌ | |
| D£® | µē³Ų³äµēŹ±¼äŌ½³¤£¬µē³ŲÖŠµÄLi2S2ĮæŌ½¶ą |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ÅØ¶Č¾łĪŖ0.1 mol•L-1µÄ HCOONaŗĶNH4Cl ČÜŅŗÖŠŃōĄė×ÓµÄĪļÖŹµÄĮæÅضČÖ®ŗĶ£ŗĒ°Õß“óÓŚŗóÕß | |
| B£® | ÓĆĻąĶ¬ÅØ¶ČµÄNaOHČÜŅŗ·Ö±šµĪ¶ØµČĢå»żpH¾łĪŖ3µÄHCOOHŗĶCH3COOHČÜŅŗÖĮÖÕµć£¬ĻūŗÄNaOHČÜŅŗµÄĢå»żĻąµČ | |
| C£® | 0.2 mol•L-1 HCOOH Óė 0.1 mol•L-1 NaOH µČĢå»ż»ģŗĻŗóµÄČÜŅŗÖŠ£ŗc£ØHCOO-£©+c£ØOH-£©=c£ØHCOOH£©+c£ØH+£© | |
| D£® | 0.2 mol•L-1 CH3COONa Óė 0.1 mol•L-1ŃĪĖįµČĢå»ż»ģŗĻŗóµÄČÜŅŗÖŠ£ØpH£¼7£©£ŗc£ØCH3COO-£©£¾c£ØCl-£©£¾c£ØCH3COOH£©£¾c£ØH+£© |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com