
【题目】现有m g某气体,它由四原子分子构成,它的摩尔质量为M gmol﹣1 , 则:
(1)该气体的物质的量为mol.
(2)该气体中所含的原子总数为个.
(3)该气体在标准状况下的体积为L.
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为 .
(5)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为molL﹣1 .
科目:高中化学 来源: 题型:
【题目】化学反应过程中发生物质变化的同时,常常伴有能量的变化.这种能量的变化常以热能的形式表现出来,叫做反应热.由于反应的情况不同,反应热可以分为许多种,如燃烧热和中和热等.
(1)下列△H表示物质燃烧热的是;表示物质中和热的是 .
A.2H2(g)+O2(g)=2H2O(l);△H1
B.C(s)+ ![]() O2(g)=CO(g);△H2
O2(g)=CO(g);△H2
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H3
D.C(s)+O2(g)=CO2(g);△H4
E.C6H12O6(s)+12O2(g)=6CO2 (g)+6H2O (l);△H5
F.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H6
G.2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l);△H7
H.CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l);△H8
(2)甲硅烷(SiH4)是一种无色液体,遇到空气能发生爆炸性自燃,生成SiO2和水.已知室温下10g甲硅烷自燃放出热量446kJ,表示其燃烧热的热化学方程式为 .
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2是放热反应,当1molCl2参与反应时释放145kJ的热量,写出这个热化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数,下列叙述正确的是( )
A.标准状况下,22.4L H2O含有的分子数为1NA
B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02NA
C.通常状况下,1NA个CO2分子占有的体积为22.4L
D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl﹣个数为1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以钡矿粉(主要成份为BaCO3 , 含有Ca2+、Fe2+、Fe3+、Mg2+等)制备BaCl22H2O的流程如图1: 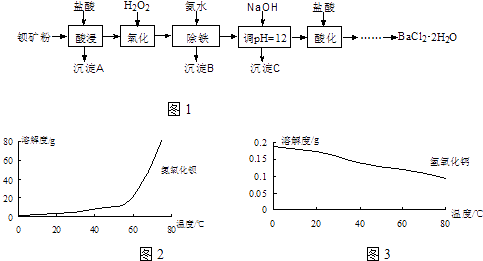
(1)氧化过程主要反应的离子方程式为 .
(2)沉淀C的主要成分是Ca(OH)2和 . 由图2可知,为了更好的使Ca2+沉淀,还应采取的措施为 .
(3)用BaSO4重量法测定产品纯度的步骤为: 步骤1:准确称取0.4~0.6g BaCl22H2O试样,加入100mL水,3mL 2molL﹣1 的HCl溶液加热溶解.
步骤2:边搅拌,边逐滴加入0.1molL﹣1 H2SO4溶液.
步骤3:待BaSO4沉降后,………..,确认已完全沉淀.
步骤4:过滤,用0.01molL﹣1的稀H2SO4洗涤沉淀3~4次,直至洗涤液中不含Cl﹣为止.
步骤5:将折叠的沉淀滤纸包置于……………中,经烘干、炭化、灰化后在800℃灼烧至恒重.称量计算BaCl22H2O中Ba2+的含量.
①步骤3所缺的操作为 .
②若步骤1称量的样品过少,则在步骤4洗涤时可能造成的影响为 .
③步骤5所用瓷质仪器名称为 . 滤纸灰化时空气要充足,否则BaSO4易被残留的炭还原生成BaS,该反应的化学方程式为 .
④有同学认为用K2CrO4代替H2SO4作沉淀剂效果更好,请说明原因 .
[已知:Ksp(BaSO4)=1.1×10﹣10 Ksp(BaCrO4)=1.2×10﹣10].
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用18molL﹣1浓硫酸配制100mL3.0molL﹣1稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积;②量取一定体积的浓硫酸;③溶解;④冷却;⑤转移、洗涤; ⑥定容、摇匀; ⑦装瓶贴标签.
完成下列问题:
(1)所需浓硫酸的体积是 , 量取浓硫酸所用的量筒的规格是(从下列中选用A.10mL B.25mL C.50mL D.100mL).
(2)第③步实验的操作是 .
(3)下列情况对所配制的稀硫酸浓度有何影响?(用“偏大”“偏小”“无影响”填写)
A.所用的浓硫酸长时间放置在密封不好的容器中;
B.容量瓶用蒸馏水洗涤后残留有少量的水;
C.所用过的烧杯、玻璃棒未洗涤;
D.定容时俯视刻度线 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一根较纯铁棒垂直没入水中,由于深水处溶氧量较少,一段时间后发现AB段产生较多铁锈,BC段腐蚀严重,下列关于此现象的说法错误的是( )
A.铁棒AB段发生反应为O2+4e﹣+2H2O=4OH﹣
B.腐蚀过程中在铁棒上会产生微电流,且方向是AB段到BC段
C.向水中加入一定量硫酸钾固体后,对铁棒的生锈速率几乎无影响
D.产生这种现象的本质原因是铁棒所处的化学环境不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表为各物质中所含的杂质以及除去这些杂质选用的试剂或操作方法,正确的是( )
物质 | 杂质 | 除杂试剂或操作方法 | |
A | CuSO4 | FeSO4 | 加入过量铁粉,过滤 |
B | NaNO3 | CaCO3 | 溶解、过滤 |
C | CO2 | O2 | 通入NaOH溶液,洗气 |
D | KNO3溶液 | AgNO3 | 加入NaCl溶液,过滤 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuI是一种不溶于水的白色固体,它可以由反应:2Cu2++4I﹣=2CuI↓+I2而得到.如图所示装置中,a、b都是惰性电极,通电一段时间后,在KI﹣淀粉溶液中阳极周围变蓝色,则下列说法正确的是( )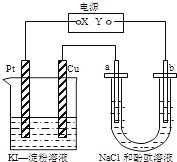
A.若a极变红,则在Pt电极上:2I﹣﹣2e﹣=I2 淀粉遇碘变蓝
B.若b极变红,在Pt电极上:4OH﹣﹣4e﹣=2H2O+O2 O2将I﹣氧化为I2 , 淀粉遇碘变蓝
C.若a极变红,在Cu电极上:开始Cu+I﹣﹣e﹣=CuI,一段时间后2I﹣﹣2e﹣═I2 淀粉遇碘变蓝
D.若b极变红,在Cu极上:Cu﹣2e﹣═Cu2+ Cu2+ 显蓝色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com