

分析 (1)①CaSO4(s)+CO(g)?CaO(s)+SO2(g)+CO2(g)△=+210.5kJ•mol-1
②$\frac{1}{4}$CaSO4(s)+CO(g)?$\frac{1}{4}$CaS(s)+CO2(g)△=-47.3kJ•mol-1
结合盖斯定律可知,②×4-①得到CaO(s)+3CO(g)+SO2(g)?CaS(s)+3CO2(g),K为生成物浓度幂之积与反应物浓度幂之积的比;
(2)发生2H2S(g)?2H2(g)+S2(g),该反应为气体体积增大的反应,增大压强平衡逆向移动,转化率减小;由图可知,温度越高,转化率越大;
(3)①平衡时物质的量不发生变化;
②反应进行至20min时,氧气的浓度瞬间增大;10min到15min的曲线斜率增大,反应速率加快,且反应物浓度减小;
(4)得到Na2SO3和NaHSO3混合溶液,且所得溶液呈中性,存在c(H+)=c(OH-),c(Na+)+c(H+)=c(OH-)+2c(SO32-)+c(HSO3-).
解答 解:(1)(1)①CaSO4(s)+CO(g)?CaO(s)+SO2(g)+CO2(g)△=+210.5kJ•mol-1
②$\frac{1}{4}$CaSO4(s)+CO(g)?$\frac{1}{4}$CaS(s)+CO2(g)△=-47.3kJ•mol-1
结合盖斯定律可知,②×4-①得到CaO(s)+3CO(g)+SO2(g)?CaS(s)+3CO2(g),
则△H=(-47.3kJ•mol-1)×4-(+210.5kJ•mol-1)=-399.7kJ/mol;
K=$\frac{{c}^{3}(C{O}_{2})}{{c}^{3}(CO)c(S{O}_{2})}$,
故答案为:-399.7;$\frac{{c}^{3}(C{O}_{2})}{{c}^{3}(CO)c(S{O}_{2})}$;
(2)图1中压强P1、P2、P3的大小顺序为P1<P2<P3;理由是反应前后气体体积增大,增大压强,平衡逆向进行;由图可知,温度越高,转化率越大,则该反应为吸热反应,升高温度,K增大,即K(T1)<K(T2),
故答案为:P1<P2<P3;反应前后气体体积增大,增大压强,平衡逆向进行;<;反应是吸热反应,升温,平衡正向进行,平衡常数增大;
(3)①平衡时物质的量不变,则反应处于平衡状态的15-20min和25-30min时间段所示,故答案为:15-20min和25-30min;
②反应进行至20min时,氧气的浓度瞬间增大,则曲线发生变化的原因是增大氧气的浓度;10min到15min的曲线斜率增大,反应速率加快,反应物浓度减小,加催化剂、缩小体积均符合,C中降低温度,反应速率减小,D中二氧化硫浓度增大,故选AB,
故答案为:增大氧气的浓度;AB;
(4)得到Na2SO3和NaHSO3混合溶液,且所得溶液呈中性,存在c(H+)=c(OH-),c(Na+)+c(H+)=c(OH-)+2c(SO32-)+c(HSO3-),则c(Na+)=2c(SO32-)+c(HSO3-),故答案为:2c(SO32-)+c(HSO3-).
点评 本题考查化学平衡的计算,为高频考点,把握盖斯定律应用、图象及平衡移动、离子浓度关系为解答的关键,侧重分析与计算能力的考查,综合性较强,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中加入AgNO3溶液,可生成白色沉淀,加稀盐酸沉淀不消失,则可确定该溶液中一定含有Cl-, | |
| B. | 用试管加热碳酸氢钠固体时试管口竖直向上 | |
| C. | 实验室需要800mL0.1mol•L-1NaOH溶液,需要称取4.0gNaOH进行配制 | |
| D. | 实验室中可用碱石灰干燥氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
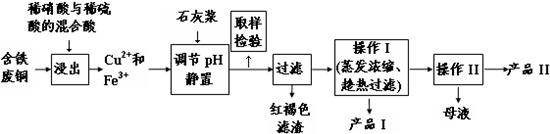
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
| 编号 | 实验操作 | 预期现象和结论 |
| ① | 在试管中加入少量FeCl3溶液和过量 (填少量、过量)的KI溶液. | 深红色如期出现 |
| ② | 将试管中的混合溶液转移至分液漏斗 (填仪器)中,倒入一定量的CCl4, 塞住活塞,充分振荡(萃取),静置. | 液体分层,上层接近无色,下层紫红色 |
| ③ | 打开活塞,先放出下层液体,再从分液漏斗的上口中倒出水层于试管中,加入KSCN溶液 | 出现血红色,则反应后的混合物中含Fe3+,进而证明这的确是一个可逆反应;反之则不含Fe3+,进而证明不是一个可逆反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | H-H | C-O | C≡C | H-O | C-H |
| E/(KJ.mol-1) | 436 | 343 | x | 465 | 413 |

查看答案和解析>>
科目:高中化学 来源: 题型:推断题

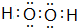 ,化合物E2 D2与化合物E2H的水溶液按物质的量比1:1反应生成单质H的离子方程式为Na2O2+2H2O+S2-=S+4Na++4OH-
,化合物E2 D2与化合物E2H的水溶液按物质的量比1:1反应生成单质H的离子方程式为Na2O2+2H2O+S2-=S+4Na++4OH-查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钡与盐酸反应 2H++BaCO3=Ba2++H2O+CO2↑ | |
| B. | 氢氧化钡溶液与稀硫酸混合 Ba2++SO42-+H++OH-=BaSO4↓+H2O | |
| C. | 氯气通入蒸馏水中 Cl2+H2O=Cl-+ClO-+2 H+ | |
| D. | CO2通入过量的澄清石灰水中 CO2+Ca(OH)2=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若生成物C、D中有一种为单质,则该反应一定是置换反应 | |
| B. | 若生成物C和D分别为两种沉淀,A、B有可能为盐和碱 | |
| C. | 若C、D是盐和水,则A、B一定是酸和碱 | |
| D. | 若C、D是两种化合物,则A、B一定是化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com