
30mL 1mol/L NaCl溶液和40mL 0.5mol/L CaCl2溶液混合后,混合液中Cl﹣浓度为()
A. 0.5mol/L B. 0.6mol/L C. 1.00mol/L D. 2mol/L
考点: 物质的量浓度的相关计算.
分析: 先利用n=cV计算各溶液中溶质的物质的量,进而计算Cl﹣的总物质的量,再根据c=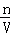 来计算混合液中Cl﹣的物质的量浓度.
来计算混合液中Cl﹣的物质的量浓度.
解答: 解:NaCl的物质的量为0.03L×1mol/L=0.03mol,
CaCl2的物质的量为0.04L×0.5mol/L=0.02mol,
则Cl﹣的物质的量为0.03mol+0.02mol×2=0.07mol,
混合溶液的体积为0.03L+0.04L=0.07L,
则混合液中Cl﹣的物质的量浓度为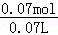 =1mol/L,
=1mol/L,
故选C.
点评: 本题考查混合溶液中离子浓度的计算,注意对物质的量浓度定义式的理解,注意溶液体积的变化忽略不计,比较基础.


 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源: 题型:
下列物质中氧原子数目与93g Na2O中氧原子数一定相等的是()
A. 67.2L CO2 B. 33g CO2 C. 80g SO3 D. 98g H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是()
A. 稀H2SO4能导电,所以稀H2SO4是电解质
B. 氧化还原反应中有一种元素化合价升高必定有另一种元素化合价降低
C. 根据是否有丁达尔效应将分散系分为溶液、胶体和浊液
D. 根据交叉分类法MgSO4既是镁盐又是硫酸盐
查看答案和解析>>
科目:高中化学 来源: 题型:
用20g烧碱配制成500mL其物质的量浓度为1mol/L,从中取出1mL,其物质的量浓度为 mol/L;含溶 质 g.若将这1mL溶液用水稀释到100mL,所得溶液中溶质的物质的量浓度为 mol/L,其中含Na+ .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是()
A. 不可将水直接倒入浓硫酸中进行稀释
B. 浓硫酸可用于干燥O2、CO2
C. 硝酸与铁反应可产生H2
D. 浓硫酸对皮肤或衣服有很强的腐蚀性
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是()
A. CO的摩尔质量为28
B. 常温常压下,NA个氢原子与NA 个氮气的质量比为1:14
C. 32克O2所含原子数目为2NA
D. 常温常压下,1molCO分子所占体积是22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
已知SO3、BF3、CCl4、PCl5、SF6都是非极性分子,而H2S、NH3、NO2、SF4、BrF5都是极性分子,由此可推出ABn型分子属于非极性分子的经验规律是( )
|
| A. | ABn型分子中A、B均不含氢原子 |
|
| B. | A元素的相对原子质量必小于B元素的相对原子质量 |
|
| C. | 分子中所有原子都在同一平面上 |
|
| D. | ABn型的价层电子对数等于n |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com