
| A、两个原子形成共价键时至少有1个σ键 |
| B、MgCl2分子中存在3个共价键 |
| C、N2分子中有2个σ键,1个π键 |
| D、键的强度大,含有该键的物质比较活泼 |


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe2O3俗称铁红,常用作红色油漆和涂料 |
| B、硅是良好的半导体材料 |
| C、二氧化硅可用于制造光导纤维 |
| D、煤炭是清洁能源,直接燃烧不会造成环境污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 组号 | 反应温度 (℃) | 参加反应的物质 | 体积(mL) | |||
| Na2S2O3 | H2SO4 | |||||
| 体积(mL) | 浓度( mol?L-1 ) | 体积(mL) | 浓度( mol?L-1) | |||
| A | 10 | 5 | 0.1 | 10 | 0.1 | 15 |
| B | 10 | 5 | 0.1 | 5 | 0.1 | 20 |
| C | 30 | 5 | 0.1 | 5 | 0.1 | 20 |
| D | 30 | 10 | 0.08 | 15 | 0.08 | 5 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
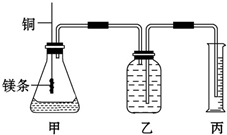 某研究性学习小组为证明在同温同压下,相同浓度相同体积的不同强度的一元酸与足量镁反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积.设计的简易实验装置如图.该实验的主要操作步骤如下:
某研究性学习小组为证明在同温同压下,相同浓度相同体积的不同强度的一元酸与足量镁反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积.设计的简易实验装置如图.该实验的主要操作步骤如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com