
 �����к��е�
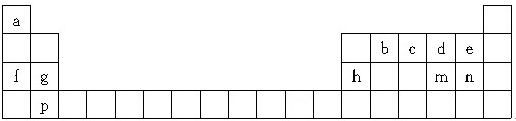
�����к��е����� ��Ԫ�������ڱ��е�λ�ã���֪aΪH��bΪC��cΪN��dΪO��eΪF��fΪNa��gΪMg��hΪAl��mΪS��nΪCl��pΪCa��
��1����m��λ�ÿ�֪��λ�����ڱ��е������ڢ�A�壻
��2��A��ͬ�����������Ԫ�طǽ�������ǿ��
B��ͬ�����������ԭ�Ӱ뾶��С��
C��SO2��CO2��Ϊ��������������������ԣ�
D��FԪ��û����ۺ����
E��a��d��ɵĻ�������H2O��H2O2�������ڹ��ۻ����f�ֱ���d��ɵĻ�������Na2O��Na2O2���������ӻ����
F���������ʵ��磬ʯīҲ���磻
��3��a��c��n��ԭ�Ӹ�����Ϊ4��1��1���ɵĻ�����NH4Cl����笠������������ӹ��ɣ�
��� �⣺��Ԫ�������ڱ��е�λ�ã���֪aΪH��bΪC��cΪN��dΪO��eΪF��fΪNa��gΪMg��hΪAl��mΪS��nΪCl��pΪCa��
��1����m��λ�ÿ�֪��λ�����ڱ��е������ڢ�A�壬�ʴ�Ϊ���������ڢ�A�壻
��2��A��ͬ�����������Ԫ�طǽ�������ǿ��b��c��dԪ�صķǽ���������ǿ����A��ȷ��
B��ͬ�����������ԭ�Ӱ뾶��С��f��g��hԪ�ص�ԭ�Ӱ뾶��С����B��ȷ��
C��SO2��CO2��Ϊ�����������ѧ�������ƣ�SԪ�ش����м��̬��CԪ�ش�����ۣ������������ԣ���C��ȷ��
D��FԪ��û����ۺ����ᣬ��D����
E��a��d��ɵĻ�������H2O��H2O2�������ڹ��ۻ�������й��ۼ���f�ֱ���d��ɵĻ�������Na2O��Na2O2���������ӻ�����������Ӽ����������ƻ����й��ۼ�����E����
F����������Na��Mg��Al��Ca���Ե��磬ʯīҲ���磬��F��ȷ��
��ѡ��ABCF��
��3��a��c��n��ԭ�Ӹ�����Ϊ4��1��1���ɵĻ�����NH4Cl����笠������������ӹ��ɣ�����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼��Ԫ�����ڱ���Ԫ�������ɣ��ѶȲ���ע������ڱ���Ԫ�������ɵ��������գ���2����Dѡ��Ϊ�״��㣬ѧ��������FԪ��û����ۺ����ᣮ


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
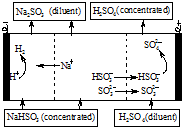 ��NaOH��Һ����SO2�������õĻ��Һ���е��ѭ�������������¹��ս�����ѭ��������������Ĥ���ѭ������������ͼ��������˵������ȷ���ǣ�������
��NaOH��Һ����SO2�������õĻ��Һ���е��ѭ�������������¹��ս�����ѭ��������������Ĥ���ѭ������������ͼ��������˵������ȷ���ǣ�������| A�� | ������������ǿ | |
| B�� | diluent��concentrated�����ĺ���ΪŨ���ġ�ϡ�͵� | |
| C�� | ���������ӵ��������ӽ���Ĥ | |
| D�� | �ù����еĸ���Ʒ��ҪΪH2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| 2 | �� | �� | �� | |||||
| 3 | �� | �� | �� | �� | �� | |||
| 4 | �� | �� |
 ��
�� ��
�� ���û���������ں��м��Լ�������ԡ��Ǽ��ԡ�����
���û���������ں��м��Լ�������ԡ��Ǽ��ԡ������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | ��Na2CO3 | ��NaHCO3 | ��Na2SiO3 | ��Na2SO3 | ��NaHSO3 | ��NaClO |
| pH | ��11.6 | 9.7�� | ��12.3 | ��10.0 | ��4.0 | ��10.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢۢ� | B�� | �ڢۢݢ� | C�� | �ڢۢܢ� | D�� | �٢ۢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ϡ���ᷴӦ��Fe2O3+6H+=2Fe2++3H2O | |
| B�� | ̼��������Һ�м�ϡ���CO32-+2H+=H2O+CO2�� | |
| C�� | ����������Һ����ϡ�����У�OH-+H+ H2O | |
| D�� | Cu��OH��2����H2SO4��2H++Cu��OH��2=Cu2++2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | S+O2�T2SO2����H=-269kJ/mol����Ӧ�ȣ� | |
| B�� | 2NO2��g���TO2��g��+2NO��g������H=+116.2kJ/mol����Ӧ�ȣ� | |
| C�� | C2H5OH��l��+3O2��g���T2CO2��g��+3H2O��g������H=-1367.0kJ/mol��ȼ���ȣ� | |
| D�� | NaOH��aq��+HCl��aq���TNaCl��aq��+H2O��l������H=+57.3kJ/mol���к��ȣ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com