
����Ŀ��CoxFe3-xO4�ŷ���һ�ֱȽϺõĸ߽������ŷۡ���FeSO4Ϊԭ���Ʊ�CoxFe3-xO4����Ҫ�������£�
![]()
��1�����������FeSO4��Һ�м���NaOH��Һ����40���½�������FeOOH���֡����ɾ��ֵĻ�ѧ����ʽΪ_____________________��
��2������ڽ������Ƶ�����FeSO4��Һ����Ƥ���������У����µ�60������������������ֳ���һ���ߴ���ˡ�ˮϴ�������FeOOH��ĩ���������з�����Ƥ��Ŀ����_______���������������Ϊ_____________________��
��3������۽�FeOOH��200��300���¼�����ˮ�����ɺ�ɫFe2O3��ʵ������ɸò�����Ҫ���������е�___________������ĸ����
a��������b���ձ�����c����������d�������ǡ���e���ƾ���
��4�������ͨ��H2��������300��400��������Fe3O4��ͨ��H2ǰҪ�����¯��ͨ��N2��������Ϊ______________________________________________��
��5��ij�о�С����������ӵ��������������LiCoO2���������������������Ʊ�CoSO4��7H2O���塣�±��г�����ؽ������������������������pH����ʼ������pH����������Ũ��Ϊ1.0 mol��L��1���㣩��
�������� | ��ʼ������pH | ������ȫ��pH |
Fe3�� | 1.1 | 3.2 |
Fe2�� | 5.8 | 8.8 |
Co2�� | 6.9 | 9.4 |
���������ʵ�鲽������ѡ�õ��Լ���H2O2��ϡ���ᡢϡ���ᡢNaOH��Һ����
����N����������ͪ��120���½�ϴ�������ϣ�ʹLiCoO2���������룬�õ�LiCoO2��Ʒ����������
�� _____________________________________________________��
�������ô�ƷCoSO4��Һ�м���NaOH��Һ������pHԼΪ5�����ˡ�
��_______________________________________________________��
�ݽ�Co��OH��2��������ϡ�����У�����Ũ�������½ᾧ���õ�CoSO4��7H2O���塣
���𰸡� 4FeSO4��8NaOH��O2![]() 4FeOOH��4Na2SO4��2H2O �������ᣬ����FeSO4 ����������������FeOOH��ʹ�������� cde ��ȥ��������ֹ������������Ϸ�Ӧ��ը ��ϡ�����ܽ�LiCoO2�����������H2O2 ���������Һ�м���NaOH��Һ������pH��9.4�����ˣ�ϴ�ӵõ�Co��OH��2����
4FeOOH��4Na2SO4��2H2O �������ᣬ����FeSO4 ����������������FeOOH��ʹ�������� cde ��ȥ��������ֹ������������Ϸ�Ӧ��ը ��ϡ�����ܽ�LiCoO2�����������H2O2 ���������Һ�м���NaOH��Һ������pH��9.4�����ˣ�ϴ�ӵõ�Co��OH��2����
��������(1)�÷�Ӧ�ķ�Ӧ��ΪFeSO4��NaOH��O2������ΪFeOOH����Ӧ�ķ���ʽΪ4FeSO4+8NaOH+O2![]() 4FeOOH+4Na2SO4+2H2O���ʴ�Ϊ��4FeSO4+8NaOH+O2
4FeOOH+4Na2SO4+2H2O���ʴ�Ϊ��4FeSO4+8NaOH+O2![]() 4FeOOH+4Na2SO4+2H2O��
4FeOOH+4Na2SO4+2H2O��
(2)�ڴ������·�Ӧ�����ᣬ�ᵼ�¾����ܽ⣬����Ӧ���ĵ����ɵ����ᣬͬʱ����ԭ��FeSO4����Һ����Ϊ+2�ۣ�ͨ�������Ϊ��������ʹ�䱻����Ϊ+3�۵������ʴ�Ϊ���������ᣬ����FeSO4������FeSO4����FeOOH��ʹ����������
(3)���ȹ��������������������������ǡ����żܡ�����ǯ���ƾ��Ƶ����ʴ�Ϊ��cde��
(4)������ȼ���������������¼��Ȼᷢ����ը�������õ����ž��������ʴ�Ϊ����ȥ��������ֹ������������Ϸ�����ը��
(5)�����ڢٷ����LiCoO2��Ʒ���ڢ۵�CoSO4��Һ����������ȥ�����ӣ��ʵڢ�Ӧ�������ܽ��Ʒ����������ɵ�����������������Ϊ�����ӣ�������˫����ˮ���ʴ�Ϊ����ϡ�����ܽ�LiCoO2�����������H2O2��
�����ڢ۵õ���������Һ���ڢ�Ӧ�õ�Co(OH)2������Ӧ��������������Һ����pH��9.4��ʹ�ܳ�����ȫ����ϴ�ӡ�����õ����������ʴ�Ϊ�����������Һ�м���NaOH��Һ������pH��9.4�����ˣ�ϴ�ӵõ�Co(OH)2������


 ���Ž�������С״Ԫϵ�д�
���Ž�������С״Ԫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����״���£��������ܱ������зֱ������������O2��O3���壬
��1������������ʵ���֮��Ϊ ��
��2������������ԭ�Ӹ���֮��Ϊ ��
��3������������ܶ�֮���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1�������м������ʣ��뽫����������пո��ڣ�
A��CH2=CH-COOH��������C17H33COOH�� B��12C60��ʯī C�� ![]() ��
��![]() D��35Cl��37Cl E���Ҵ����Ҷ���
D��35Cl��37Cl E���Ҵ����Ҷ���
�ٻ�Ϊͬλ�ص���______________���ڻ�Ϊͬϵ�����_________________��
�ۻ�Ϊͬ�����������__________���ܻ�Ϊͬ���칹�����_____________��
�ݼȲ���ͬϵ��ֲ���ͬ�����壬Ҳ����ͬ�������壬���ɿ�����ͬһ�����ʵ���______
��2����д�����з�Ӧ�Ļ�ѧ����ʽ��
�ٱ����������γɶ��ģ�____________________________________________________________
�ڵ���ˮ�⣺______________________________________________________________________
�۱�ȩ�����Ƶ�������ͭ����Һ��Ӧ��________________________________________________
��3����֪������֬�Ľṹ��ʽ����ͼ��ʾ����д���ϳɵ�����֬����Ҫ����Ľṹ��ʽ��
 ________________��_________________
________________��_________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��µĶ����ܱ������з�����ӦH2(g)+I2(g)![]() 2HI(g)��������˵����Ӧ�Ѿ��ﵽƽ��״̬����
2HI(g)��������˵����Ӧ�Ѿ��ﵽƽ��״̬����
A. ������ÿ����1mol I2��ͬʱ����2mol HI
B. ����������ѹǿ���ٱ仯
C. ����������ɫ���ٱ仯
D. ���������ܶȲ��ٱ仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.������Mg5Al3��OH��19��H2O��4������������ȼ���ϣ�����ʱ�����»�ѧ����ʽ�ֽ⣺2Mg5Al3��OH��19��H2O��4 ![]() 27H2O��+10MgO+3Al2O3
27H2O��+10MgO+3Al2O3
���Բ���A��������Ԫ����ɵĻ����ij�о�С�鰴��ͼ����̽������ɣ�
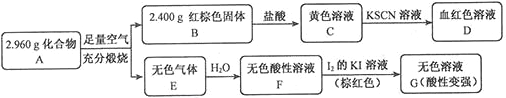
��1��A�����Ԫ��Ϊ_________����Ԫ�ط��ű�ʾ������ѧʽΪ______��
��2����ҺC���ܽ�ͭƬ���оٸ÷�Ӧ��һ��ʵ��Ӧ��____________��
��3����֪������A����ϡ���ᷴӦ������һ�ֵ���ɫ�������һ�����壨����µ��ܶ�Ϊ1.518 g��L-1������������ӵĵ���ʽΪ____��д���÷�Ӧ�����ӷ���ʽ__________��
��4��д��F��G��Ӧ�Ļ�ѧ����ʽ_____________�����ʵ�鷽��̽����ҺG�е���Ҫ����������H2O��H+��K+��I-��______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ���ں��д���PbI2�ı�����Һ�д�����ƽ��PbI2(s)![]() Pb2+(aq)+ 2I (aq)������ŨKI��Һ������˵����ȷ����
Pb2+(aq)+ 2I (aq)������ŨKI��Һ������˵����ȷ����
A. ��Һ��Pb2+��IŨ�ȶ����� B. �ܶȻ�����Ksp����
C. �����ܽ�ƽ�������ƶ� D. ��Һ��Pb2+Ũ�ȼ�С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ�����ӷ���ʽ��ȷ����
A. HCO3����H2O![]() H3O+��CO32�� B. NH4����H2O
H3O+��CO32�� B. NH4����H2O![]() NH3��H2O��H��
NH3��H2O��H��
C. CO32����2H2O![]() H2CO3��2OH�� D. Fe3����3H2O
H2CO3��2OH�� D. Fe3����3H2O![]() Fe(OH)3����3H��
Fe(OH)3����3H��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ΪV L����������Һ�м��������İ�ˮ�����˵ó�����������ϴ�����������������ٱ仯ʱ��ȴ����������mg��ɫ���壮ԭ��Һ��c��SO42����Ϊ�� ��
A.![]() mol?L��1
mol?L��1
B.![]() mol?L��1
mol?L��1
C.![]() mol?L��1
mol?L��1
D.![]() mol?L��1
mol?L��1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com