
”¾ĢāÄæ”潫ĶŠæŗĻ½šČܽāŗóÓė×ćĮæKIČÜŅŗ·“Ó¦£ØZn2+²»ÓėI-·“Ó¦£©£¬Éś³ÉµÄI2ÓĆNa2S2O3±ź×¼ČÜŅŗµĪ¶Ø£¬øł¾ŻĻūŗĵÄNa2S2O3ČÜŅŗĢå»żæɲāĖćŗĻ½šÖŠĶµÄŗ¬Į攣ŹµŃé¹ż³ĢČēĻĀĶ¼ĖłŹ¾£ŗ

»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©H2O2µÄµē×ÓŹ½ĪŖ_________£»”°Čܽā”±ŗóĶŌŖĖŲµÄÖ÷ŅŖ“ęŌŚŠĪŹ½ŹĒ______£ØĢīĄė×Ó·ūŗÅ£©”£
£Ø2£©”°Öó·Š”±µÄÄæµÄŹĒ³żČ„¹żĮæµÄH2O2”£298KŹ±£¬ŅŗĢ¬¹żŃõ»ÆĒā·Ö½ā£¬ĆæÉś³É0.01molO2·Å³öČČĮæ1.96kJ£¬øĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ_______________”£
£Ø3£©ÓĆ»ŗ³åČÜŅŗ”°µ÷PH”±ŹĒĪŖĮĖ±ÜĆāČÜŅŗµÄĖįŠŌĢ«Ē棬·ńŌņ”°µĪ¶Ø”±Ź±·¢Éś·“Ó¦£ŗ
S2O32-£«2H+=S”ż£«SO2”ü+H2O
¢Ł øĆ»ŗ³åČÜŅŗŹĒÅØ¶Č¾łĪŖ0.10mol/LµÄCH3COOHŗĶCH3COONH4µÄ»ģŗĻČÜŅŗ”£25”ꏱ£¬ČÜŅŗÖŠø÷ÖÖĄė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņĪŖ_________”£
[ŅŃÖŖ£ŗ25”ꏱ£¬Ka(CH3COOH)=Kb(NH3”¤H2O)=1.8”Į10-5]
¢Ś Čō100 mL Na2S2O3ČÜŅŗ·¢ÉśÉĻŹö·“Ó¦Ź±£¬20sŗóÉś³ÉµÄSO2±ČS¶ą3.2g£¬Ōņv(Na2S2O3)=_____mol/(L”¤s)£ØŗöĀŌČÜŅŗĢå»ż±ä»ÆµÄÓ°Ļģ£©”£
£Ø4£©”°³Įµķ”±²½ÖčÖŠÓŠCuI³Įµķ²śÉś£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ_____________”£
£Ø5£©”°×Ŗ»Æ”±²½ÖčÖŠ£¬CuI×Ŗ»ÆĪŖCuSCN£¬CuSCNĪüø½I2µÄĒćĻņ±ČCuIøüŠ”£¬Ź¹”°µĪ¶Ø”±Īó²ī¼õŠ””£³ĮµķĶźČ«×Ŗ»Æŗó£¬ČÜŅŗÖŠc(SCN -):c(I-)”Ż_______________”£
£ŪŅŃÖŖ£ŗKsp(CuI)=1.1”Į10-12£»Ksp(CuSCN)=4.4”Į10-15]
£Ø6£©ĻĀĮŠĒéæöæÉÄÜŌģ³É²āµĆµÄĶŗ¬ĮæĘ«øߵďĒ______£ØĢī±źŗÅ£©”£
A. ĶŠæŗĻ½šÖŠŗ¬ÉŁĮæĢś
B. ”°³Įµķ”±Ź±£¬I2ÓėI-½įŗĻÉś³ÉI3- :I2+I£=I3-
C. ”°×Ŗ»Æ”±ŗóµÄČÜŅŗŌŚæÕĘųÖŠ·ÅÖĆĢ«¾Ć£¬Ć»ÓŠ¼°Ź±µĪ¶Ø
D. ”°µĪ¶Ø”±¹ż³ĢÖŠ£¬Ķł×¶ŠĪĘæÄŚ¼ÓČėÉŁĮæÕōĮóĖ®
”¾“š°ø”æ ![]() Cu2+ 2H2O2(l)=O2(g)”ü+2H2O(l) ”÷H=-196kJ/mol c(CH3COO-)”¢c(NH4+)”¢c(H+)”¢c(OH-) 0.050 2Cu2++4I-=2CuI+I2 4.0”Į10-3 A”¢C
Cu2+ 2H2O2(l)=O2(g)”ü+2H2O(l) ”÷H=-196kJ/mol c(CH3COO-)”¢c(NH4+)”¢c(H+)”¢c(OH-) 0.050 2Cu2++4I-=2CuI+I2 4.0”Į10-3 A”¢C
”¾½āĪö”æ£Ø1£©H2O2ŹĒ¹²¼Ū»ÆŗĻĪļ£¬µē×ÓŹ½ĪŖ![]() £»”°Čܽā”±ŗóĶ±»Ńõ»ÆĪŖĶĄė×Ó£¬Ņņ“ĖĶŌŖĖŲµÄÖ÷ŅŖ“ęŌŚŠĪŹ½ŹĒCu2+”££Ø2£©298KŹ±£¬ŅŗĢ¬¹żŃõ»ÆĒā·Ö½ā£¬ĆæÉś³É0.01molO2·Å³öČČĮæ1.96kJ£¬Ņņ“ĖøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ2H2O2(l)=O2”ü(g)+2H2O(l) ”÷H=-196kJ/mol”££Ø3£©¢Łøł¾ŻµēĄė³£ŹżæÉÖŖļ§øłŗĶ“×ĖįøłµÄĖ®½ā³Ģ¶ČĻąĶ¬£¬Ņņ“Ė“×Ėįļ§ČÜŅŗĻŌÖŠŠŌ£¬ĖłŅŌ10mol/LµÄCH3COOHŗĶCH3COONH4µÄ»ģŗĻČÜŅŗÖŠø÷ÖÖĄė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņĪŖc(CH3COO-)£¾c(NH4+)£¾c(H+)£¾c(OH-)”£¢Śøł¾Ż·½³ĢŹ½S2O32-£«2H+=S”ż£«SO2”ü+H2OæÉÖŖÉś³É1molSO2±Č1molSµÄÖŹĮæ¶ą32g£¬20sŗóÉś³ÉµÄSO2±ČS¶ą3.2g£¬Ņņ“ĖŹĒSŹĒ0.1mol£¬ĻūŗÄĮņ“śĮņĖįÄĘŹĒ0.1mol£¬ÅØ¶ČŹĒ1mol/L£¬ĖłŅŌv(Na2S2O3)=1mol/L”Ā20s£½0.050mol/(L”¤s)”££Ø4£©”°³Įµķ”±²½ÖčÖŠÓŠCuI³Įµķ²śÉś£¬·“Ó¦ÖŠĶĄė×ÓŃõ»ÆµāĄė×ÓÉś³Éµ„ÖŹµā£¬×ŌÉķ±»»¹ŌĪŖCuI£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ2Cu2++4I-=2CuI+I2”££Ø5£©³ĮµķĶźČ«×Ŗ»Æŗó£¬ČÜŅŗÖŠc(SCN -):c(I-)”ŻKsp(CuSCN)£ŗKsp(CuI)=4.4”Į10-15/1.1”Į10-12=4.0”Į10-3”££Ø6£©A.ĶŠæŗĻ½šÖŠŗ¬ÉŁĮæĢś£¬·“Ó¦ÖŠ×Ŗ»ÆĪŖĢśĄė×Ó£¬ĢśĄė×ÓÄÜŃõ»Æµ„ÖŹµā£¬µ¼ÖĀĻūŗıź×¼ŅŗĢå»żŌö¼Ó£¬²ā¶Ø½į¹ūĘ«øߣ¬AÕżČ·£»B.”°³Įµķ”±Ź±£¬I2ÓėI-½įŗĻÉś³ÉI3- :I2+I£=I3-£¬Ōģ³É±ź×¼ŅŗĢå»ż¼õŠ”£¬²ā¶Ø½į¹ūĘ«µĶ£¬B“ķĪó£»C.”°×Ŗ»Æ”±ŗóµÄČÜŅŗŌŚæÕĘųÖŠ·ÅÖĆĢ«¾Ć£¬µ¼ÖĀĮņ“śĮņĖįÄʱäÖŹ£¬Ļūŗıź×¼ŅŗĢå»żŌö¼Ó£¬²ā¶Ø½į¹ūĘ«øߣ¬CÕżČ·£»D.”°µĪ¶Ø”±¹ż³ĢÖŠ£¬Ķł×¶ŠĪĘæÄŚ¼ÓČėÉŁĮæÕōĮóĖ®²»Ó°Ļģ²ā¶Ø½į¹ū£¬D“ķĪ󣬓š°øŃ”AC”£
£»”°Čܽā”±ŗóĶ±»Ńõ»ÆĪŖĶĄė×Ó£¬Ņņ“ĖĶŌŖĖŲµÄÖ÷ŅŖ“ęŌŚŠĪŹ½ŹĒCu2+”££Ø2£©298KŹ±£¬ŅŗĢ¬¹żŃõ»ÆĒā·Ö½ā£¬ĆæÉś³É0.01molO2·Å³öČČĮæ1.96kJ£¬Ņņ“ĖøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ2H2O2(l)=O2”ü(g)+2H2O(l) ”÷H=-196kJ/mol”££Ø3£©¢Łøł¾ŻµēĄė³£ŹżæÉÖŖļ§øłŗĶ“×ĖįøłµÄĖ®½ā³Ģ¶ČĻąĶ¬£¬Ņņ“Ė“×Ėįļ§ČÜŅŗĻŌÖŠŠŌ£¬ĖłŅŌ10mol/LµÄCH3COOHŗĶCH3COONH4µÄ»ģŗĻČÜŅŗÖŠø÷ÖÖĄė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņĪŖc(CH3COO-)£¾c(NH4+)£¾c(H+)£¾c(OH-)”£¢Śøł¾Ż·½³ĢŹ½S2O32-£«2H+=S”ż£«SO2”ü+H2OæÉÖŖÉś³É1molSO2±Č1molSµÄÖŹĮæ¶ą32g£¬20sŗóÉś³ÉµÄSO2±ČS¶ą3.2g£¬Ņņ“ĖŹĒSŹĒ0.1mol£¬ĻūŗÄĮņ“śĮņĖįÄĘŹĒ0.1mol£¬ÅØ¶ČŹĒ1mol/L£¬ĖłŅŌv(Na2S2O3)=1mol/L”Ā20s£½0.050mol/(L”¤s)”££Ø4£©”°³Įµķ”±²½ÖčÖŠÓŠCuI³Įµķ²śÉś£¬·“Ó¦ÖŠĶĄė×ÓŃõ»ÆµāĄė×ÓÉś³Éµ„ÖŹµā£¬×ŌÉķ±»»¹ŌĪŖCuI£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ2Cu2++4I-=2CuI+I2”££Ø5£©³ĮµķĶźČ«×Ŗ»Æŗó£¬ČÜŅŗÖŠc(SCN -):c(I-)”ŻKsp(CuSCN)£ŗKsp(CuI)=4.4”Į10-15/1.1”Į10-12=4.0”Į10-3”££Ø6£©A.ĶŠæŗĻ½šÖŠŗ¬ÉŁĮæĢś£¬·“Ó¦ÖŠ×Ŗ»ÆĪŖĢśĄė×Ó£¬ĢśĄė×ÓÄÜŃõ»Æµ„ÖŹµā£¬µ¼ÖĀĻūŗıź×¼ŅŗĢå»żŌö¼Ó£¬²ā¶Ø½į¹ūĘ«øߣ¬AÕżČ·£»B.”°³Įµķ”±Ź±£¬I2ÓėI-½įŗĻÉś³ÉI3- :I2+I£=I3-£¬Ōģ³É±ź×¼ŅŗĢå»ż¼õŠ”£¬²ā¶Ø½į¹ūĘ«µĶ£¬B“ķĪó£»C.”°×Ŗ»Æ”±ŗóµÄČÜŅŗŌŚæÕĘųÖŠ·ÅÖĆĢ«¾Ć£¬µ¼ÖĀĮņ“śĮņĖįÄʱäÖŹ£¬Ļūŗıź×¼ŅŗĢå»żŌö¼Ó£¬²ā¶Ø½į¹ūĘ«øߣ¬CÕżČ·£»D.”°µĪ¶Ø”±¹ż³ĢÖŠ£¬Ķł×¶ŠĪĘæÄŚ¼ÓČėÉŁĮæÕōĮóĖ®²»Ó°Ļģ²ā¶Ø½į¹ū£¬D“ķĪ󣬓š°øŃ”AC”£


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A. ŅŌæÉÄę·“Ó¦ĪŖŌĄķµÄŌµē³Ų·¢Éś·“Ó¦“ļĘ½ŗāŹ±£¬øƵē³ŲČŌÓŠµēĮ÷²śÉś
B. ĻņAgCl”¢AgBrµÄ±„ŗĶČÜŅŗÖŠ¼ÓČėÉŁĮæµÄAgNO3£¬ČÜŅŗÖŠĀČĄė×ÓŗĶäåĄė×ÓÅØ¶ČµÄ±ČÖµ²»±ä
C. Ź¹ÓĆ“ß»Æ¼ĮÄܹ»½µµĶ·“Ó¦µÄ”÷H
D. ½šŹō·¢ÉśĪüŃõøÆŹ“Ź±£¬±»øÆŹ“µÄĖŁĀŹŗĶŃõÅضČĪŽ¹Ų
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŃĒĻõĖįÄĘ£ØNaNO2£©ÓŠĻńŹ³ŃĪŅ»ŃłµÄĻĢĪ¶£¬±»³ĘĪŖ¹¤ŅµŃĪ”£ŅŃÖŖ£ŗŃĒĻõĖįŹĒČõĖį£¬ĒŅNO+NO2 +2NaOH=2NaNO2+H2O”£Ä³Ķ¬Ń§¾Ż“ĖČĻĪŖNaNO2æÉÓėĮņĖį·“Ó¦£¬ĒŅÓŠNOŗĶNO2Éś³É£¬²¢ÓūÓĆĻĀĶ¼ĖłŹ¾ŅĒĘ÷£Ø¼Š³Ö×°ÖĆŅŃŹ”ĀŌ£©¼°Ņ©Ę·£¬ŃéÖ¤×Ō¼ŗµÄ¼ŁÉč”£ŅŃÖŖ·Šµć£ŗNO2ĪŖ21”ę£¬NOĪŖ-151”ę

£Ø1£©ÉĻŹöŅĒĘ÷µÄĮ¬½ÓĖ³ŠņĪŖ£ŗA”ś____”ś_____”ś_____”śB”£
£Ø2£©·“Ó¦Ē°£¬ĻČ“ņæŖµÆ»É¼Š£¬ĶØČėŅ»¶ĪŹ±¼äµŖĘų£¬ĘäÄæµÄŹĒ____________”£
£Ø3£©¹Ų±ÕµÆ»É¼Š£¬“ņæŖ·ÖŅŗĀ©¶·»īČū£¬µĪČė70%ĮņĖįŗó£¬AÖŠ²śÉśĮĖŗģ×ŲÉ«ĘųĢ壬
¢Ł ŅĄ¾Ż___________________ĻÖĻó£¬æÉČ·ČĻ²śĪļÖŠÓŠNO
¢Ś ×°ÖĆEµÄ×÷ÓĆŹĒ_________________”£
£Ø4£©Čē¹ūƻӊװÖĆC£¬¶ŌŹµŃé½įĀŪµÄÓ°ĻģŹĒ____________________”£
£Ø5£©×ŪŗĻŅŌÉĻŠÅĻ¢ĶʶĻ£¬NO2ÓėNaOHČÜŅŗ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_______________”£
£Ø6£©¼ŗÖŖ£ŗ2NaNO2+4HI=2NaI+I2+2NO+2H2O£¬øł¾ŻÕāŅ»·“Ó¦£¬æÉŅŌÓĆŹŌ¼ĮŗĶÉś»īÖŠµÄ³£¼ūĪļÖŹ¼ų±šŃĒĻõĖįÄĘŗĶŹ³ŃĪ£¬½ųŠŠŹµŃ鏱£¬±ŲŠėŃ”ÓƵÄĪļÖŹÓŠ__________________”£
A.×ŌĄ“Ė® B.µā»Æ¼ŲČÜŅŗ C.µķ·Ū D.°×ĢĒ E. Ź³“× F.°×¾Ę
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø12·Ö£©äå±½ŹĒŅ»ÖÖ³£ÓĆµÄ»Æ¹¤ŌĮĻ£¬Ķس£ŅŌ±½ŗĶäåĪŖŌĮĻÖĘČ”£¬²é׏ĮĻÖŖ£ŗ
±½ | äå | äå±½ | |
ĆܶČ/g”¤cm£3 | 0£®88 | 3£®10 | 1£®50 |
·Šµć/”ę | 80 | 59 | 156 |
ŌŚĖ®ÖŠµÄČܽā¶Č | Ī¢ČÜ | Ī¢ČÜ | Ī¢ČÜ |
ŹµŃéŹŅÖʱøäå±½µÄŹµŃé²½ÖčČēĻĀ£ŗ
²½Öč1£ŗŌŚaÖŠ¼ÓČė15 mL±½ŗĶÉŁĮæĢśŠ¼£¬ŌŁ½«bÖŠ4£®0 mLŅŗäåĀżĀż¼ÓČėµ½aÖŠ”£
²½Öč2£ŗ³ä·Ö·“Ó¦ŗó£¬ĻņaÖŠ¼ÓČė10 mLĖ®£¬Č»ŗó¹żĀĖ³żČ„Ī“·“Ó¦µÄĢśŠ¼”£
²½Öč3£ŗĀĖŅŗŅĄ“ĪÓĆ10 mLĖ®”¢8 mL 10%µÄNaOHČÜŅŗ”¢10 mL Ė®Ļ“µÓ£¬·ÖŅŗµĆ“Öäå±½”£
²½Öč4£ŗĻņ·Ö³öµÄ“Öäå±½ÖŠ¼ÓČėÉŁĮæµÄĪŽĖ®ĀČ»ÆøĘ£¬¾²ÖĆ”¢¹żĀĖ¼“µĆ“Ö²śĘ·”£

£Ø1£©²½Öč1ŅĒĘ÷aÖŠ·¢ÉśµÄÖ÷ŅŖ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ£ŗ ”£
£Ø2£©ŅĒĘ÷cµÄ×÷ÓĆŹĒĄäÄż»ŲĮ÷£¬»ŲĮ÷µÄÖ÷ŅŖĪļÖŹÓŠ£ŗ ”£
£Ø3£©²½Öč3ÖŠNaOHĖł·¢ÉśµÄÖ÷ŅŖ·“Ó¦ŹĒ£ŗ ”£
£Ø4£©Čō½«Ķ¼1ŠéĻßæņ²æ·ÖøÄĪŖĶ¼2×°ÖĆ£¬Ōņ D”¢EæÉŅŌ¼ģŃé³öĄ“µÄĪļÖŹŹĒ £¬ĘäÖŠŹŌ¹ÜCÖŠ±½µÄ×÷ÓĆŹĒ £¬ÄÜ·ń¾Ż“ĖÅŠ¶Ļ·¢ÉśĮĖČ”“ś·“Ó¦£æ £ØĢī”°ŹĒ”±»ņ”°·ń”±£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚt ”ꏱ£¬AgBrŌŚĖ®ÖŠµÄ³ĮµķČܽāĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾”£ÓÖÖŖt ”ꏱAgClµÄKsp£½4”Į10£10£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
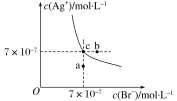
A£®ŌŚt ”ꏱ£¬AgBrµÄKspĪŖ4.9”Į10£13
B£®ŌŚAgBr±„ŗĶČÜŅŗÖŠ¼ÓČėNaBr¹ĢĢ壬æÉŹ¹ČÜŅŗÓÉcµć±äµ½bµć
C£®Ķ¼ÖŠaµć¶ŌÓ¦µÄŹĒAgBr µÄ²»±„ŗĶČÜŅŗ
D£®ŌŚt ”ꏱ£¬AgCl(s)£«Br£(aq) ![]() AgBr(s)£«Cl£(aq)µÄĘ½ŗā³£ŹżK”Ö816
AgBr(s)£«Cl£(aq)µÄĘ½ŗā³£ŹżK”Ö816
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ½üÄźĄ“AIST±ØøęÕżŌŚŃŠ¾æŅ»ÖÖ”°øßČŻĮ攢µĶ³É±¾”±ļ®ĶæÕĘųČ¼ĮĻµē³Ų”£øƵē³ŲĶعżŅ»ÖÖø“ŌÓµÄĶøÆŹ“”°ĻÖĻó”±²śÉśµēĮ¦£¬ĘäÖŠ·Åµē¹ż³ĢĪŖ2Li+Cu2O+H2O![]() 2Cu+2Li++2OH£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
2Cu+2Li++2OH£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ

A. ·ÅµēŹ±£¬øŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖCu2O+H2O+2e![]() 2Cu+2OH
2Cu+2OH
B. ·ÅµēŹ±£¬Li+Ķø¹ż¹ĢĢåµē½āÖŹĻņCu¼«ŅʶÆ
C. ĶØæÕĘųŹ±£¬Ķ±»øÆŹ“£¬±ķĆę²śÉśCu2O
D. Õūøö·“Ó¦¹ż³ĢÖŠ£¬ĶĻąµ±ÓŚ“߻ƼĮ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹ°“µē½āÖŹ”¢·Ēµē½āÖŹ”¢»ģŗĻĪļÅÅŠņÕżČ·µÄŹĒ£Ø £©
A£®ĪåĖ®ĮņĖįĶ”¢H2SO4”¢æÕĘų B£®NH3”¢Cu”¢ČÜŅŗ
C£®ŃĪĖį”¢SO2”¢½ŗĢå D£®“æ¼ī”¢ŅŅ“¼”¢ĢśæóŹÆ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŅ»¶ØĪĀ¶ČĻĀ£¬½«µČĮæµÄĘųĢåZ·Ö±šĶØČėĘšŹ¼Ģå»żĻąĶ¬µÄĆܱÕČŻĘ÷¢ń(ŗćČŻ)ŗĶ¢ņ(ŗćŃ¹)ÖŠ£¬Ź¹Ęä·¢Éś·“Ó¦£¬t0Ź±ČŻĘ÷¢ńÖŠ“ļµ½»ÆŃ§Ę½ŗā£¬X”¢Y”¢ZµÄĪļÖŹµÄĮæÓėŹ±¼äµÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾£¬ŌņĻĀĮŠÓŠ¹ŲĶʶĻÕżČ·µÄŹĒ (””””)

A. øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ3X£«2Y![]() 3Z
3Z
B. ČōĮ½ČŻĘ÷ÖŠ¾ł“ļµ½Ę½ŗāŗó£¬Ģå»żV(¢ń)<V(¢ņ)£¬ŌņČŻĘ÷¢ņ“ļµ½Ę½ŗāĖłÓĆŹ±¼äŠ”ÓŚt0
C. ČōĮ½ČŻĘ÷ÖŠ¾ł“ļµ½Ę½ŗāŗó£¬ĒŅX”¢Y”¢Z¾łĪŖĘųĢ¬£¬ŌņZµÄĢå»ż·ÖŹż¢ń>¢ņ
D. “ļĘ½ŗāŗó£¬Čō¶ŌČŻĘ÷¢ņÉżøßĪĀ¶ČŹ±ĘäĢå»żŌö“ó£¬ĖµĆ÷Z·¢ÉśµÄ·“Ó¦ĪŖĪüČČ·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ»śĪļŌŚŹŹĮæµÄÅØ¶ČŹ±£¬Ķس£²»ÄÜÓĆӌɱ¾ś”¢Ļū¶¾µÄŹĒ£Ø £©
A. ±½·ÓČÜŅŗB. ŅŅ“¼ČÜŅŗC. ¼×Č©ČÜŅŗD. ŅŅĆŃČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com