
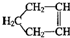
 可简写为
可简写为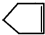 ,降冰片烯的分子结构可表示为:
,降冰片烯的分子结构可表示为: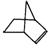
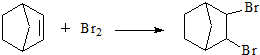 ,故答案为:
,故答案为: ;
;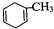 ,
, .
.


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
| A、氯化钾溶液在电流作用下电离成K+和Cl- |
| B、氧化还原反应的本质是有化合价的升降 |
| C、依据丁达尔效应可将分散系分为溶液、胶体与浊液 |
| D、硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第二位 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| 催化剂 |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸工业中SO2转化为SO3时采用常压,是因为增大压强不会提高SO2的转化率 |
| B、打开啤酒瓶的瓶盖,有大量的气泡冒出来,该现象不能用勒夏特列原理解释 |
| C、氯碱工业中用离子交换膜电解槽电解时,往阴极室注入经过精制的饱和NaCl溶液,往阳极室注入稀氢氧化钠溶液(或去离子水) |
| D、工业上合成氨采用500℃左右的温度,最主要原因是该反应的催化剂在500℃左右时活性最好 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、葡萄糖和淀粉均属于高分子化合物 |
| B、鸡蛋清中加入 CuSO4 溶液会产生盐析 |
| C、14C可用于文物年代的鉴定,14C与14N互为同位素 |
| D、自由移动离子数目多的电解质溶液导电能力不一定强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
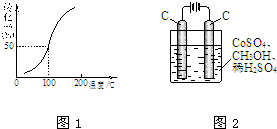 甲醇可作电池的原料,也会造成环境污染.请根据有关反应回答问题.
甲醇可作电池的原料,也会造成环境污染.请根据有关反应回答问题.| 1 |
| 2 |
| c(H2) |
| c(CH3OH) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com