
| 氯气 |
| ① |
| 一定条件 |
| ② |
| 高温、高压、催化剂 |
| ③ |
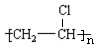 ,则乙为CH2=CHCl,反应②是ClCH2CH2Cl发生消去反应生成乙(CH2=CHCl),反应方程式为:ClCH2CH2Cl
,则乙为CH2=CHCl,反应②是ClCH2CH2Cl发生消去反应生成乙(CH2=CHCl),反应方程式为:ClCH2CH2Cl| 一定条件 |
| 一定条件 |
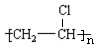 .
.


科目:高中化学 来源: 题型:
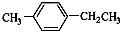 )是一种重要的有机原料,用该物质可合成其他物质.
)是一种重要的有机原料,用该物质可合成其他物质.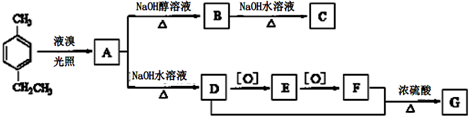
查看答案和解析>>
科目:高中化学 来源: 题型:
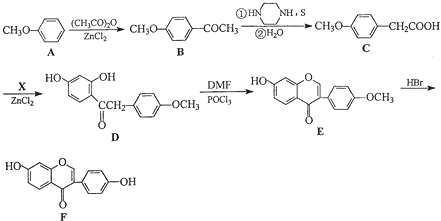
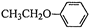 和(CH3CO)2O为原料制备药物中间体
和(CH3CO)2O为原料制备药物中间体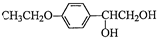 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C=CH2
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C=CH2| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验次数 | 镁带质量(g) | 测得气体的体积(L) |
| 1 | 18.000 | 16.90 |
| 2 | 18.000 | 17.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
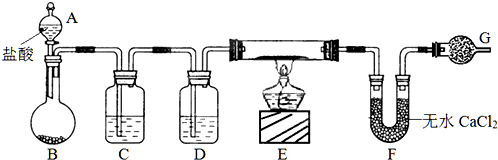
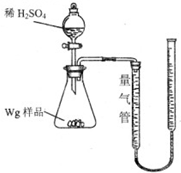 用如图所示装置测定Fe和Fe2O3的混合物中单质铁的质量分数(夹持部分已略去).称取Wg样品置于锥形瓶中,通过分液漏斗加入足量稀硫酸使样品完全溶解.实验前量气管起始读数为amL,实验后量气管的最终读数为bmL.
用如图所示装置测定Fe和Fe2O3的混合物中单质铁的质量分数(夹持部分已略去).称取Wg样品置于锥形瓶中,通过分液漏斗加入足量稀硫酸使样品完全溶解.实验前量气管起始读数为amL,实验后量气管的最终读数为bmL.| 序号 | 溶液中可能存在 的金属离子 | 选择最少种数的试剂,验证该 假设(填字母) |
| ① | ||
| ② | ||
| ③ |
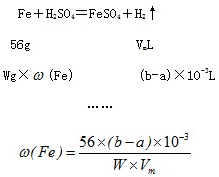
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
| B | AgI沉淀中滴入稀KCl溶液 | 有白色沉淀出现 | AgCl比AgI更难溶 |
| C | 常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸 | 有气泡产生 | 不能说明常温下Kap(BaCO3)与Kap(BaSO4)的大小关系 |
| D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com