
【题目】在一定温度下,将2molA和2molB两种气体相混合于容积为2L的某密闭容器中,发生如下反应:3A(g)+B(g) ![]() xC(g)+2D(g),2min后反应达平衡状态,生成0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
xC(g)+2D(g),2min后反应达平衡状态,生成0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)x值等于____;
(2)A的转化率为______;
(3)生成D的反应速率为___________;
(4)如果增大体系的压强,则平衡体系中C的质量分数_____(填“增大”、“减小”或“不变”)。
【答案】2 60% 0.2mol/(L·min) 不变
【解析】
由题意2min后反应达平衡状态,生成0.8molD建立如下三段式:
3A(g)+B(g) ![]() xC(g)+2D(g)
xC(g)+2D(g)
起始量(mol) 2 2 0 0
转化量(mol) 1.2 0.4 0.4x 0.8
平衡量(mol) 0.8 1.6 0.4x 0.8
(1)由三段式可知,平衡时C的物质的量为0.4x,由题意可知C的浓度为0.4mol/L,则可得0.4mol/L×2L=0.4xmol,解得x=2,故答案为:2;
(2)由三段式数据可知A的转化率为![]() ×100%=60%,故答案为:60%;
×100%=60%,故答案为:60%;
(3)由三段式数据可知生成D的反应速率为![]() =0.2mol/(L·min),故答案为:0.2mol/(L·min);
=0.2mol/(L·min),故答案为:0.2mol/(L·min);
(4)该反应是一个反应前后体积不变的反应,增大反应体系的压强,平衡不移动,平衡体系中C的质量分数不变,故答案为:不变;


科目:高中化学 来源: 题型:
【题目】中国化学家研究的一种新型复合光催化剂[碳纳米点(CQDs)/氮化碳(C3N4)纳米复合物]可以利用太阳光实现高效分解水,其原理如图所示。下列说法正确的是
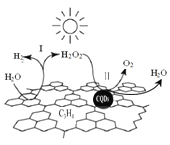
A. C3N4中C的化合价为 -4
B. 反应的两个阶段均为吸热过程
C. 阶段Ⅱ中,H2O2既是氧化剂,又是还原剂
D. 通过该反应,实现了化学能向太阳能的转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,对应的现象以及结论均正确的是( )
选项 | 实验操作 | 实验现象 | 结论 |
A | 取少量Na2SO3固体于试管中,加水溶解,滴加Ba(NO3)2溶液,再滴加稀硝酸 | 滴加Ba(NO3)2溶液,产生白色沉淀,再滴加稀硝酸,沉淀不溶解 | Na2SO3固体已经变质 |
B | 将SO2通入酸性KMnO4溶液中 | 溶液的紫红色褪去 | SO2具有漂白性 |
C | 将铁片投入浓硫酸中 | 无明显变化 | 常温下铁不与浓硫酸反应 |
D | 将10mL2mol/L的KI溶液与1mL1mol/LFeCl3溶液混合充分反应后滴加KSCN溶液 | 溶液颜色变红 | KI与FeCl3的反应具有可逆性 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不同条件下进行合成氨的反应N2(g)+3H2(g) ![]() 2NH3(l),根据下列在相同时间内测定的结果判断生成氨的速率最快的是( )
2NH3(l),根据下列在相同时间内测定的结果判断生成氨的速率最快的是( )
A.v(H2)=0.1mol/(L·min)B.v(N2)=0.1mol/(L·min)
C.v(N2)=0.2mol/(L·min)D.v(NH3)=0.3mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L密闭容器内,800 ℃时反应2NO(g)+O2(g)![]() 2NO2(g) ΔH<0,n(NO)随时间的变化如下表:
2NO2(g) ΔH<0,n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)下图中表示NO2的变化的曲线是_____。用O2表示从0~2 s内该反应的平均速率v=____。

(2)能说明该反应已达到平衡状态的是____。
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.v逆(NO)=2v正(O2) D.容器内密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各情况,在其中Fe片腐蚀由快到慢的顺序是( )
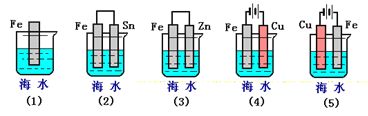
A. (5)(2)(1)(3)(4) B. (2)(5)(3)(4)(1)
C. (5)(3)(4)(1)(2) D. (1)(5)(3)(4)(2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.中和热测定实验中需要的玻璃仪器有:烧杯、量筒、温度计、环形玻璃搅拌棒
B.乙烯的燃烧热为1411.3 kJ·mol1,则乙烯燃烧的热化学方程式为C2H4(g)+3O2(g)![]() 2CO2(g)+2H2O(g) ΔH= 1411.3 kJ·mol1
2CO2(g)+2H2O(g) ΔH= 1411.3 kJ·mol1
C.用石墨电极电解1 L 0.1 mol·L1 CuSO4溶液,若反应产生0.1 mol O2,则向原溶液中加入0.2 mol CuO能恢复至原浓度
D.用pH试纸分别测定氯水和盐酸的pH,比较两溶液的酸性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】捕获二氧化碳生成甲酸的过程如图所示。下列说法正确的是(NA为阿伏加德罗常数的值)
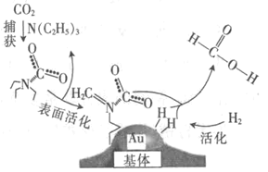
A.标准状况下,22.4 L CO2中所含的电子数目为16NA
B.10.1 g N(C2H5)3中所含的极性共价键数目为2.1NA
C.2 mol Au与2 mol H2中所含的分子数目均为2NA
D.100 g 46%的甲酸水溶液中所含的氧原子数目为5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池,如图所示。
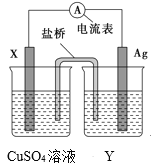
请回答下列问题:
(1)电极X的材料是___;电解质溶液Y是___。
(2)银电极为电池的___极,发生的电极反应为___。X电极上发生的电极反应为___。
(3)外电路中的电子是从____极流向___极。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com