
| A. | 第二周期ⅡA族 | B. | 第三周期ⅡA族 | C. | 第三周期ⅢA族 | D. | 第二周期ⅢA族 |
分析 金属与酸反应置换出氢气,金属提供电子,根据氧化还原反应电子转移守恒,计算金属的物质的量.结合生成的氯化物中含有电子的物质的量,求出金属含有的电子数,进而确定金属元素在元素周期表中的位置.
解答 解:氢气的物质的量为$\frac{0.5g}{2g/mol}$=0.25mol;
令金属为nmol,根据电子转移守恒有:
2×n=0.25mol×2,解得n=0.25,
生成的氯化物中共有11.5mol电子,则1mol氯化物中含有的电子数为$\frac{11.5}{0.25}$=46mol,则1个M含有的电子数为46-17×2=12;
所以M为12号元素Mg,位于第三周期ⅡA族;
故选:B
点评 本题考查通过计算推断元素,难度中等,注意从氧化剂、还原剂得失电子的数目关系判断金属元素原子失去电子数目是解题的关键.


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 78gNa2O2晶体中所含离子数约为1.806×1024 | |
| B. | 4.48L氨气分子中含0.6NA个N-H键 | |
| C. | PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构 | |
| D. | N2H4分子中极性键和非极性键的比值为1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.6g Fe和足量的盐酸反应时,失去的电子数为0.3NA | |
| B. | 1 mol Na2O2固体中含离子总数为3NA | |
| C. | 标准状况下,22.4 L SO3所含分子数为NA | |
| D. | 0.5mol/L的MgCl2溶液中,含有Cl- 个数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
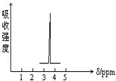 化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图如图所示,则A的结构简式为:CH2BrCH2Br,预测B的核磁共振氢谱上有2个峰.
化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图如图所示,则A的结构简式为:CH2BrCH2Br,预测B的核磁共振氢谱上有2个峰.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 .下列有关二甲醚的叙述正确的是( )
.下列有关二甲醚的叙述正确的是( )| A. | 二甲醚是一种有机物,属于非电解质 | |
| B. | 4.6g该物质中含有共价键的数目为2×6.02×1022 | |
| C. | 二甲醚和乙醇互为同分异构体且和甲醇互为同系物 | |
| D. | 标准状况下,燃烧11.2L二甲醚一定生成22.4LCO2 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省长春市高二上学期期初考试化学试卷 题型:实验题
某强碱性溶液中可能含有的离子是K+、NH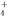 、Al3+、AlO
、Al3+、AlO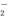 、SO
、SO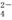 、SiO
、SiO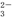 、CO
、CO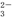 、Cl-中的某几种离子,现进行如下实验:
、Cl-中的某几种离子,现进行如下实验:
①取少量的溶液用硝酸酸化后,加Ba(NO3)2溶液,无沉淀生成;
②另取少量溶液加入盐酸,其现象是:一段时间保持原样后,开始产生沉淀并逐渐增多,沉淀量基本不变后产生一种气体,最后沉淀逐渐减少至消失。
(1)原溶液中肯定存在 的离子是,肯定不存在的离子是。
的离子是,肯定不存在的离子是。
(2)已知一定量的原溶液中加入5mL0.2mol/L盐酸时,沉淀会完全消失,加入足量的硝酸银溶液可得到沉淀0.187g,则原溶液中是否含有Cl- ?。
(3)按照反应顺序逐步书写出②中发生反应的离子反应方程式
①H++OH-=H2O②
③
④HCO3-+H+=H2O+CO2↑
⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com