

 .
. .
.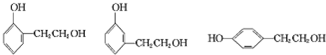 .
.分析 烃A和溴发生加成反应生成B,B和氢氧化钠的水溶液发生取代反应生成C,根据C的分子式知,C是HOCH2CH2OH,则B是BrCH2CH2Br,A是乙烯.D为烃,质谱图表明G的相对分子质量为166,其中含碳元素57.8%,含氢元素3.6%,其余为氧元素,则D分子中碳原子个数为$\frac{166×57.8%}{12}$=8,H原子数目为$\frac{166×3.6%}{1}$=6,O原子数目为$\frac{166-12×8-6}{16}$=4,故G的分子式为C8H6O4,G能与NaHCO3溶液反应,说明G中含有羧基,G分子中含有两种类型的氢原子,且G中含有苯环,则G的结构简式为: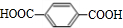 ,由转化关系可知,F为
,由转化关系可知,F为 ,E的结构简式为:
,E的结构简式为: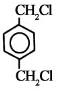 ,D为
,D为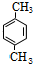 ,乙二醇和对二苯甲酸反应生成聚酯纤维H为
,乙二醇和对二苯甲酸反应生成聚酯纤维H为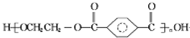 ,据此解答.
,据此解答.
解答 解:烃A和溴发生加成反应生成B,B和氢氧化钠的水溶液发生取代反应生成C,根据C的分子式知,C是HOCH2CH2OH,则B是BrCH2CH2Br,A是乙烯.D为烃,质谱图表明G的相对分子质量为166,其中含碳元素57.8%,含氢元素3.6%,其余为氧元素,则D分子中碳原子个数为$\frac{166×57.8%}{12}$=8,H原子数目为$\frac{166×3.6%}{1}$=6,O原子数目为$\frac{166-12×8-6}{16}$=4,故G的分子式为C8H6O4,G能与NaHCO3溶液反应,说明G中含有羧基,G分子中含有两种类型的氢原子,且G中含有苯环,则G的结构简式为: ,由转化关系可知,F为
,由转化关系可知,F为 ,E的结构简式为:
,E的结构简式为: ,D为
,D为 ,乙二醇和对二苯甲酸反应生成聚酯纤维H为
,乙二醇和对二苯甲酸反应生成聚酯纤维H为 .
.
(1)反应①属于加成反应,反应③属于取代反应,故答案为:加成反应;取代反应;
(2)由上述分析可知,B是BrCH2CH2Br,名称为1,2-二溴乙烷,E的结构简式为 ,
,
故答案为:1,2-二溴乙烷; ;
;
(4)反应②的化学反应方程式为:BrCH2CH2Br+2NaOH$→_{△}^{水}$HOCH2CH2OH+2NaBr;
反应⑥的化学反应方程式为: ,
,
故答案为:BrCH2CH2Br+2NaOH$→_{△}^{水}$HOCH2CH2OH+2NaBr; ;
;
(5)F( )有多种同分异构体,同时符合下列条件的同分异构体:
)有多种同分异构体,同时符合下列条件的同分异构体:
a.含有苯环且苯环上只有2个取代基,b.能与NaOH溶液反应,含有酚羟基,c.在Cu催化下与O2反应的产物能发生银镜反应,含有醇羟基,符合条件的同分异构体有: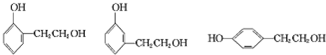 ,
,
故答案为: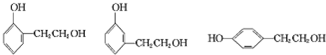 .
.
点评 本题考查有机物的推断、有机反应类型、同分异构体书写等,注意根据反应条件及有机物分子式进行推断,需要学生熟练掌握官能团的性质与转化,难度中等.


科目:高中化学 来源: 题型:填空题
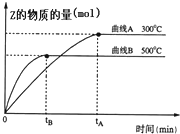 向a L密闭容器中加入1mol X气体和2mol Y气体,发生如下反应:X(g)+2Y(g)?2Z(g),不同温度下,测得平衡状态Z的物质的量变化曲线如图所示.
向a L密闭容器中加入1mol X气体和2mol Y气体,发生如下反应:X(g)+2Y(g)?2Z(g),不同温度下,测得平衡状态Z的物质的量变化曲线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将高锰酸钾晶体加热分解,所得固体质量减少 | |
| B. | 观察氯化钾溶液没有颜色,表明溶液中K+无色 | |
| C. | 在氯化钾溶液中加入适量锌粉振荡,静置后未见明显变化,表明锌与K+无反应 | |
| D. | 在高锰酸钾溶液中加入适量锌粉振荡,静置后见紫红色褪去,表明MnO4-离子为紫红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+ | B. | Ca2+ | C. | Mg2+ | D. | Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 铜的平均溶解速率 (×10-3mol•L-1•min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH均为9的①Na2CO3溶液、②CH3COONa溶液、③NaOH溶液,其物质的量浓度的大小顺序为①>②>③ | |
| B. | 等物质的量浓度的Na2CO3溶液和NaHCO3溶液等体积混合,所得溶液中:c(CO32-)+c(OH-)<c(H+)+c(HCO3-)+3c(H2CO3) | |
| C. | 0.1 mol•L-1KHC2O4溶液中:c(OH-)=c(H+)+c(H2C2O4)-2c(C2O42-) | |
| D. | pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液:c(R2-)+c(HR-)=c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某化学兴趣小组对碳的氧化物做了深入的研究并取得了一些成果.
某化学兴趣小组对碳的氧化物做了深入的研究并取得了一些成果.| 实验组序 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
| H2O | CO | CO2 | |||
| 1 | 500 | 4 | 8 | 3.2 | 4 |
| 2 | 750 | 2 | 4 | 0.8 | 3 |
| 3 | 750 | 2 | 4 | 0.8 | 1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com