
| A£® | ·“Ó¦¢ŁŹĒ¼Ó³É·“Ó¦ | B£® | Ö»ÓŠ·“Ó¦¢ŚŹĒ¼Ó¾Ū·“Ó¦ | ||
| C£® | Ö»ÓŠ·“Ó¦¢ßŹĒČ”“ś·“Ó¦ | D£® | ·“Ó¦¢ŪŹĒŃõ»Æ·“Ó¦ |
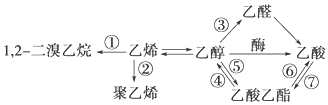
·ÖĪö ÓÉĶ¼ÖŠ×Ŗ»ÆæÉÖŖ£¬¢ŁĪŖĻ©ĢžµÄ¼Ó³É·“Ó¦£¬¢ŚĪŖ¼Ó¾Ū·“Ó¦£¬¢ŪĪŖ“ß»ÆŃõ»Æ·“Ó¦£¬¢Ż¢ßĪŖõ„»Æ·“Ó¦£¬¢Ü¢ŽĪŖĖ®½ā·“Ó¦£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗA£®·“Ó¦¢ŁŅŅĻ©Óėäå·¢ÉśµÄ¼Ó³É·“Ó¦£¬¹ŹAÕżČ·£»
B£®·“Ó¦¢ŚĪŖŅŅĻ©·¢Éś¼Ó¾Ū·“Ӧɜ³É¾ŪŅŅĻ©£¬¹ŹBÕżČ·£»
C£®Ė®½ā”¢õ„»Æ·“Ó¦¾łĪŖČ”“ś·“Ó¦£¬Ōņ¢Ü¢Ż¢Ž¢ßĪŖČ”“ś·“Ó¦£¬¹ŹC“ķĪó£»
D£®ÓÉÉĻŹö·ÖĪöæÉÖŖ£¬Ö»ÓŠ·“Ó¦¢ŪŹĒŃõ»Æ·“Ó¦£¬¹ŹDÕżČ·£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļµÄŗĻ³É£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕ¹ŁÄÜĶűä»Æ”¢ÓŠ»ś·“Ó¦ĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬עŅāÓŠ»śĪļŠŌÖŹµÄÓ¦ÓĆ£¬ĢāÄæÄŃ¶Č²»“ó£®


 æŚĖćĢāæØŗÓ±±ÉŁÄź¶łĶƳö°ęÉēĻµĮŠ“š°ø
æŚĖćĢāæØŗÓ±±ÉŁÄź¶łĶƳö°ęÉēĻµĮŠ“š°ø A¼Ó½šĢā ĻµĮŠ“š°ø
A¼Ó½šĢā ĻµĮŠ“š°ø Č«ÓŲāŹŌ¾ķĻµĮŠ“š°ø
Č«ÓŲāŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
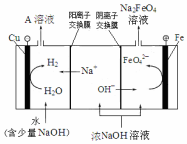 øßĢśĖį¼Ų£ØK2FeO4£©ŹĒŅ»ÖÖŠĀŠĶ”¢øߊ§”¢¶ą¹¦ÄÜĖ®“¦Ąķ¼Į£®
øßĢśĖį¼Ų£ØK2FeO4£©ŹĒŅ»ÖÖŠĀŠĶ”¢øߊ§”¢¶ą¹¦ÄÜĖ®“¦Ąķ¼Į£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŃęÉ«·“Ó¦ŹĒ»ĘÉ« | |
| B£® | ČÜŅŗÓŠĻĢĪ¶ | |
| C£® | ȔɣĮæČÜŅŗÓŚŹŌ¹ÜÖŠ£¬µĪ¼ÓĻ”ĻõĖįĖį»ÆµÄĻõĖįŅųČÜŅŗ£¬³öĻÖ°×É«³Įµķ | |
| D£® | ¼Č³öĻÖAÖŠµÄĻÖĻó£¬ÓÖ³öĻÖCÖŠµÄĻÖĻó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ”°Īķ”±ŹĒĪ¢Š”Ė®µĪ»ņ±ł¾§×é³ÉµÄĘųČܽŗĻµĶ³ | |
| B£® | ”°ö²”±ÖŠµÄ»Ņ³¾¶Ō“óĘųÖŠµÄÓŠŗ¦ĪļÖŹĘšĪüø½×÷ÓĆ | |
| C£® | Īķö²ÖŠµÄ¶žŃõ»ÆĮņ”¢µŖŃõ»ÆĪļÖ÷ŅŖĄ“×ŌÓŚ»ÆŹÆČ¼ĮĻµÄČ¼ÉÕ | |
| D£® | Īķö²ÖŠµÄÓŠ»śĢ¼Ēā»ÆŗĻĪļÖ÷ŅŖĄ“×ŌÓŚÉśĪļÖŹµÄČ¼ÉÕ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ²ā¶ØŠņŗÅ | NaHCO3ČÜŅŗµÄĢå»ż/mL | ŃĪĖį±ź×¼ŅŗµĪ¶Ø¹ÜÖŠµÄ¶ĮŹż/mL | |
| µĪ¶ØĒ° | µĪ¶Øŗó | ||
| 1 | 20.00 | 1.50 | 21.52 |
| 2 | 20.00 | 1.80 | 25.62 |
| 3 | 20.00 | 0.20 | 20.18 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | HNO3”śNO | B£® | H2SO4 £ØÅØ£©”śSO2 | C£® | I-”śI2 | D£® | Br2”śBr- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na2CO3+CaCl2ØTCaCO3”ż+2NaCl | B£® | Fe+CuSO4ØTCu+FeSO4 | ||
| C£® | 2NaHCO3ØTNa2CO3+CO2”ü+H2O | D£® | CaO+H2OØTCa£ØOH£©2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
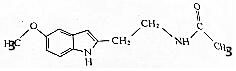 ij±£½”Ę·ÄŌ°×½š°ü×°ŗŠÄŚø½ÓŠŅ»ÕŲśĘ·ĖµĆ÷Źé£¬ĘäÖŠøų³öĮĖøĆ²śĘ·µÄÖ÷ŅŖ³É·ÖµÄ½į¹¹¼ņŹ½£ØČēĶ¼£©£®
ij±£½”Ę·ÄŌ°×½š°ü×°ŗŠÄŚø½ÓŠŅ»ÕŲśĘ·ĖµĆ÷Źé£¬ĘäÖŠøų³öĮĖøĆ²śĘ·µÄÖ÷ŅŖ³É·ÖµÄ½į¹¹¼ņŹ½£ØČēĶ¼£©£®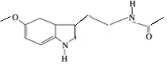 £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com