
【题目】38.4gCu跟适量的浓HNO3反应,Cu全部反应后共收集到气体22.4L(标准状况),反应中作氧化剂的硝酸与总消耗的HNO3的物质的量比( )
A. 5∶11 B. 6∶11 C. 5∶6 D. 6∶5
【答案】A
【解析】
n(Cu)=![]() =0.6mol,n(气体)=
=0.6mol,n(气体)=![]() =1mol,由生成硝酸铜的物质的量可以知道表现酸性的硝酸的物质的量,由气体的物质的量可得被还原的硝酸的物质的量,以此计算反应消耗的硝酸的物质的量,计算反应中作氧化剂的硝酸与总消耗的HNO3的物质的量比。
=1mol,由生成硝酸铜的物质的量可以知道表现酸性的硝酸的物质的量,由气体的物质的量可得被还原的硝酸的物质的量,以此计算反应消耗的硝酸的物质的量,计算反应中作氧化剂的硝酸与总消耗的HNO3的物质的量比。
铜的物质的量为:n(Cu)=![]() =0.6mol,生成气体的物质的量为: n(气体)=
=0.6mol,生成气体的物质的量为: n(气体)=![]() =1mol,则被还原的硝酸的物质的量为1mol;
=1mol,则被还原的硝酸的物质的量为1mol;
则生成n[Cu(NO3)2]的物质的量为0.6mol,可以知道表现酸性的硝酸的物质的量为0.6mol![]() 2=1.2mol,
2=1.2mol,
所以参加反应的硝酸的物质的量为:1mol+1.2mol=2.2mol, 则反应中作氧化剂的硝酸与总消耗的HNO3的物质的量比为1mol:2.2mol=5:11,
所以A选项是正确的。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】按要求完成下列问题:
(1)写出下列反应的化学方程式:
①乙烯通入到溴的四氯化碳溶液中:_____________________。
②苯与浓硝酸、浓硫酸混合后加热至50℃~60℃发生反应:__________________。
(2)给下列有机物命名:
①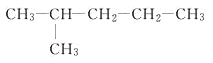 _______________________
_______________________
②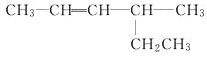 _____________________
_____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
①少量Cl2通入FeI2溶液中:Cl2+2I=2Cl+I2
②Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
③向次氯酸钙溶液中通入少量SO2:Ca2++2ClO+H2O+SO2=CaSO3↓+2HClO
④FeBr2溶液与等物质的量Cl2反应:2Fe2++2Br+2Cl2=2Fe3++4Cl+Br2
⑤向小苏打溶液中加入过量的澄清石灰水:HCO+Ca2++OH=CaCO3↓+H2O
⑥硫酸氢钠溶液与足量氢氧化钡溶液混合:H++SO![]() +Ba2++OH=BaSO4↓+H2O
+Ba2++OH=BaSO4↓+H2O
⑦Na2O2与H2O反应制备O2:Na2O2+H2O=2Na++2OH+O2↑
A. ①②⑤⑦ B. ①②③⑥ C. ③④⑤⑦ D. ①④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为电化学降解NO![]() 。下列说法中正确的是( )
。下列说法中正确的是( )
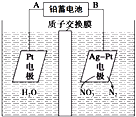
A. 铅蓄电池的A极为阴极
B. 电解的过程中有H+从右池移动到左池
C. 该电解池的阴极反应为:2NO3- + 6H2O + 12e- = N2↑ + 12OH-
D. 若电解过程中转移1moL电子,则交换膜两侧电解液的质量变化差为7.2g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证铜与稀硝酸反应的还原产物是NO而不是NO2,设计了如下图的装置,以下叙述错误的是
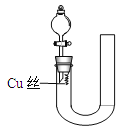
A. 应先打开活塞再从右侧加稀硝酸
B. 左侧稀硝酸须注满
C. 关闭活塞后铜丝会全部溶解
D. 反应停止后打开活塞气体变成红棕色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M是二苯乙炔类液晶材料的一种,最简单的二苯乙炔类化合物是![]() 。以互为同系物的单取代芳烃A、G为原料合成M的一种路线(部分反应条件略去)如下:
。以互为同系物的单取代芳烃A、G为原料合成M的一种路线(部分反应条件略去)如下:
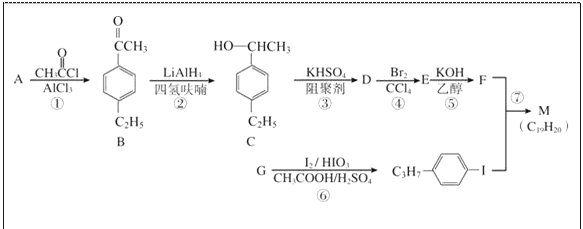
回答下列问题:
(1)A的分子式为____________。
(2)D中含有的官能团是____________,分子中最多有____________个碳原子共平面。
(3)①的反应类型是____________,③的反应类型是____________。
(4)⑤的化学方程式为________________________________________________。
(5)B的同分异构体中能同时满足如下条件:①苯环上有两个取代基,②能发生银镜反应,共有________种(不考虑立体异构),其中核磁共振氢谱为5组峰,且峰面积比为6:2:2:1:1的是________(写结构简式)。
(6)参照上述合成路线,设计一条由苯乙烯和甲苯为起始原料制备![]() 的合成路线: _____________。
的合成路线: _____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氧化还原反应的叙述正确的是( )
A. 化合反应和复分解反应不可能是氧化还原反应
B. 阳离子只能得到电子被还原,阴离子只能失去电子被氧化
C. 含有最高价元素的化合物不一定具有很强的氧化性
D. 在氧化还原反应中肯定有一种元素被氧化,另一种元素被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料。
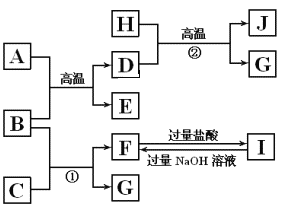
根据图示回答问题:
(1)写出下列物质的化学式:A ______,E______;
(2)反应①的化学方程式是_________________________ ;
反应②的化学方程式是___________________________ ;
(3)J与盐酸反应的化学方程式是______________________ ;
反应后的溶液与足量的D反应的离子方程式是______________________,如何检验最后溶液中的阳离子:______________________________________。
(4)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com