
【题目】对于平衡体系:aA(g)+bB(g)![]() cC(g)+dD(g) △H<0,下列判断其中不正确的是
cC(g)+dD(g) △H<0,下列判断其中不正确的是
A. 若温度不变,容器体积扩大一倍,此时A的浓度是原来的0.45倍,则a+b<c+d
B. 若从正反应开始,平衡时,A、B的转化率相等,则投入A、B的物质的量之比为a:b
C. 若平衡体系中共有气体Mmol,再向其中充入bmolB,达到平衡时气体总物质的量为( M+b)mol,则a+b=c+d
D. 若a+b=c+d,对于体积不变的容器,升高温度,平衡向左移动,容器中气体的压强不变
【答案】D
【解析】A项,温度不变,容器体积扩大一倍,此时A的浓度是原来的0.45倍,说明降低压强,化学平衡向正反应方向移动,又因为降低压强化学平衡向气体分子数增大的方向移动,故a+b<c+d,故A正确;B项,若A、B的初始物质的量之比等于化学计量数之比,平衡时A、B的转化率一定相等,所以若从正反应开始,平衡时,A、B的转化率相等,则投入A、B的物质的量之比为a:b,故B正确;C项,平衡体系中共有气体Mmol,再向其中充入bmolB,化学平衡正向移动,达到平衡时气体总物质的量为(M+b)mol,则混合气体的总的物质的量不变,故反应前后气体的化学计量数之和相等,即a+b=c+d,故C正确;D项,若a+b=c+d,气体的物质的量不变,对于体积不变的容器,温度升高,气体压强增大,故D错误。


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
【题目】有下列8种物质,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是( )
①甲烷②苯③聚乙烯④1,3-丁二烯⑤2-丁炔⑥邻二甲苯⑦乙醛⑧环己烯.
A. ①③④⑤⑧B. ①④⑤⑧C. ④⑤⑦⑧D. ①③④⑤⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】连二次硝酸(H2N2O2)是一种二元酸,可用于制N2O气体。
(1)连二次硝酸中氮元素的化合价为________。
(2)常温下,用0.01mol·L-1的NaOH溶液滴定10mL0.01mol·L-1的H2N2O2溶液,测得溶液的pH与NaOH客液体积的关系如图所示。

①写出H2N2O2在水溶液中的电离方程式:________。
②b点时溶液中c(H2N2O2)________c(N2O22-)。(填“>”“<”或“=”下同)
③a点时溶液中c(Na+)________c(HN2O2-)+c(N2O22-)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 开启啤酒瓶后,瓶中马上泛起大量泡沫
B. 合成氨反应,为提高氨的产率,理论上应采取降低温度的措施
C. 工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
D. 对于2HI(g)![]() H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深
H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化锂(LiH)在干燥的空气中能稳定存在,遇水或酸能够引起燃烧。某活动小组准备使用下列装置制备LiH固体。
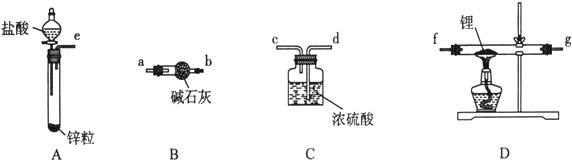
甲同学的实验方案如下:
(1)仪器的组装连接:上述仪器装置按气流从左到右连接顺序为________________,加入药品前首先要进行的实验操作是____________(不必写出具体的操作方法);其中装置B的作用是___________。
(2)添加药品:用镊子从试剂瓶中取出一定量金属锂(固体石蜡密封),然后在甲苯中浸洗数次,该操作的目的是____________________,然后快速把锂放入到石英管中。
(3)通入一段时间氢气后加热石英管,通氢气的作用是___________________________;在加热D处的石英管之前,必须进行的实验操作是__________。
(4)加热一段时间后,停止加热,继续通氢气冷却,然后取出LiH,装入氮封的瓶里,保存于暗处。采取上述操作的目的是为了避免LiH与空气中的水蒸气接触而发生危险,反应方程式为_____________。
(5)准确称量制得的产品0.174g,在一定条件下与足量水反应后,共收集到气体470.4 mL(已换算成标准状况),则产品中LiH与Li的物质的量之比为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)配平该方程式__KMnO4+__HCl (浓) =__KCl+__MnCl2+__Cl2↑+__H2O
(2)反应中(1)中____是还原剂,_____是还原产物 .
(3)该反应的离子方程式为:_______________________
(4)用双线桥法分析此氧化还原反应____________________________
(5)NA表示阿伏伽德罗常数,若产生标准状况下的气体的体积为2.24L ,则反应过程中转移电子的数目为_________,被氧化的HCl的质量为_____g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中,在碱性溶液里能大量共存,并且溶液为无色透明的是( )
A.K+ MnO4- Cl- SO42-B.Na+ K+ Al3+ Ba2+
C.Na+ HCO3- NO3- SO42-D.Na+ SO42- S2- Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物材料衍生物2,5-呋喃二甲酸(![]() )可以替代化石燃料衍生物对苯二甲酸,与乙二醇合成材料聚2,5-呋喃二甲酸乙二醇酯(PEF)。下列说法正确的是
)可以替代化石燃料衍生物对苯二甲酸,与乙二醇合成材料聚2,5-呋喃二甲酸乙二醇酯(PEF)。下列说法正确的是
A. 合成PEF的反应为加聚反应
B. PEF不能与氢气发生加成反应
C. 通过红外光谱法测定PEF的平均相对分子质量,可得其聚合度
D. 聚对苯二甲酸乙二醇酯的结构简式为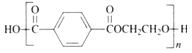
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com