
| A. | X、Y元素的主族序数之差为1 | |
| B. | 若X+、Y2-相差两个电子层,则X2Y可能是离子化合物也可能是共价化合物 | |
| C. | 若X+、Y2-核外电子数相差8,则原子半径Y>X | |
| D. | 若X+、Y2-具有相同的电子层结构,则离子半径X+>Y2- |
分析 由离子所带电荷可知X为ⅠA族元素,Y为ⅥA族元素,若X+、Y2-相差两个电子层,如X应为H,则Y为O,如X为Li,则Y为S,若X+、Y2-具有相同的电子层结构,X位于Y的下一周期,以此解答该题.
解答 解:由离子所带电荷可知X为ⅠA族元素,Y为ⅥA族元素,
A.X为ⅠA族元素,Y为ⅥA族元素,X、Y元素的主族序数之差为5,故A错误;
B.若X+、Y2-相差两个电子层,如X应为H,则Y为O,如X为Li,则Y为S,则X2Y可能是离子化合物也可能是共价化合物,故B正确;
C.若X+、Y2-核外电子数相差8,如X的原子序数大,则X的原子半径大,故C错误;
D.若X+、Y2-具有相同的电子层结构,X位于Y的下一周期,核电荷数越大离子半径越小,故D错误.
故选B.
点评 本题考查结构性质位置关系应用,侧重对元素周期律的考查,关键是结合原子序数确定元素,注意对基础知识的理解掌握.


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
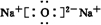 、
、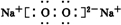 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 硼镁泥是一种工业废料,主要成份是MgO,还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业.从硼镁泥中提取MgSO4•7H2O的流程如下:
硼镁泥是一种工业废料,主要成份是MgO,还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业.从硼镁泥中提取MgSO4•7H2O的流程如下: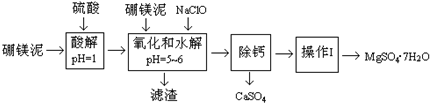
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 2.3 | 4.0 | 7.6 |
| 完全沉淀pH | 4.1 | 5.2 | 9.6 |
| 温度(℃) | 20 | 40 | 50 | 60 | 70 |
| MgSO4 | 25.0 | 31.8 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.256 | 0.212 | 0.207 | 0.201 | 0.190 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1}{1}H$和$\frac{2}{1}H$互为同位素 | B. | 淀粉和纤维素互为同分异构体 | ||
| C. | 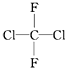 和 和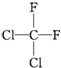 属于同一种物质 属于同一种物质 | D. | C2H6和C4H10互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

 .
. ,其名称为3-乙基戊烷.
,其名称为3-乙基戊烷.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
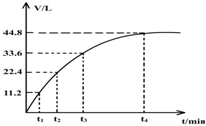 向一洁净干燥的烧杯中加入44.4gAl粉与Fe粉混合物,然后加入过量的盐酸,产生标况下气体26.88L.若将该混合物加入500ml15mol•L-的浓HNO3中(不考虑发生钝化),产生的气体(标准状况下测定)如图所示,假设HNO3的还原产物为NO与NO2,那么理论上从哪一时刻开始产生NO气体.( )
向一洁净干燥的烧杯中加入44.4gAl粉与Fe粉混合物,然后加入过量的盐酸,产生标况下气体26.88L.若将该混合物加入500ml15mol•L-的浓HNO3中(不考虑发生钝化),产生的气体(标准状况下测定)如图所示,假设HNO3的还原产物为NO与NO2,那么理论上从哪一时刻开始产生NO气体.( )| A. | t1 | B. | t2 | C. | t3 | D. | t4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li2NH中N的化合价是-1 | B. | LiH的电子式为Li+:H- | ||
| C. | 该反应中H2既是氧化剂又是还原剂 | D. | LiNH2是还原产物,LiH是氧化产物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com