
【题目】下列离子方程式正确的是
A. 硫酸氢钠溶液与小苏打溶液的反应:H+ + HCO3- = CO2↑ + H2O
B. 用苛性钠溶液吸收过量SO2:SO2 +2OH-= SO32- + H2O
C. 二氧化锰和浓盐酸反应:MnO2+4HCl![]() Mn2++2Cl2↑+2H2O
Mn2++2Cl2↑+2H2O
D. 工业上氯气和石灰乳反应制漂白粉:Cl2 + 2OH-= ClO-+ Cl- + H2O
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:高中化学 来源: 题型:
【题目】聚硅酸铁是目前无机高分子絮凝剂研究的热点,一种用钢管厂的废铁渣(主要成分Fe3O4,少量C及SiO2)为原料制备的流程如下:
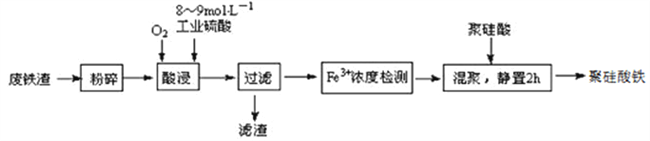
已知:在一定温度下酸浸时Fe3+在pH=2开始沉淀,pH=3.7沉淀完全
(1)废铁渣进行“粉碎”的目的是___________________________________________________。
(2)“酸浸”需适宜的酸浓度、液固比、酸浸温度、氧流量等,其中酸浸温度对铁浸取率的影响如下表所示:
温度℃ | 40 | 60 | 80 | 100 | 120 |
铁浸取率 | 50 | 62 | 80 | 95 | 85 |
①请写出酸浸过程中Fe3O4发生的离子反应方程式__________________________________。
②硫酸酸浸时应控制溶液的pH____________,其原因是_________________________________。
③当酸浸温度超过100℃时,铁浸取率反而减小,其原因是___________________。
(3)上述过滤步骤的滤液的主要成分为____________(填化学式)。
(4)Fe3+浓度定量检则,是先用SnCl2将Fe3+还原为Fe2+;在酸性条件下,再用K2Cr2O7标准溶液滴定Fe2+(Cr2O72-被还原为Cr3+),该滴定反应的离子方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解Na2PbCl4溶液,生成Pb,装置如下图,下列说法不正确的是
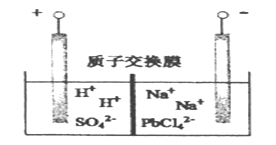
A. 阴极的电极反应式为 PbCl42- +2e- =Pb + 4Cl-
B. 电解一段时间后,Na2PbCl4浓度极大下降,可加入PbO恢复其浓度
C. 电解过程中阳极溶液的pH减小,阴极的pH保持不变
D. 电路中通过0.2mol,则阴极的质量增加20.7g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】脱水环化是合成生物碱类天然产物的重要步骤,某生物碱V合成路线如下:
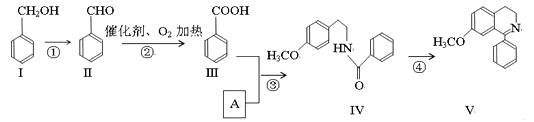
(1)写出Ⅳ中含氧官能团的名称_____________________。
(2)写出Ⅳ物质的分子式_____________。
(3)写出下列反应的类型②___________,③________________。
(4)反应②的化学方程式___________________________________。
(5)Ⅰ和Ⅲ在浓硫酸催化加热时反应的化学方程式__________________________。
(6)A的结构简式_______________________。
(7)Ⅵ与Ⅰ互为同分异构体,Ⅵ遇FeCl3发生显色反应,其苯环上的一氯代物只有2种。写出满足上述条件的Ⅵ的结构简式________________________。
(8)一定条件下,化合物Ⅶ(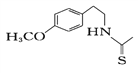 )也能发生类似反应④的环化反应,Ⅶ的环化产物的结构简式__________________________________。
)也能发生类似反应④的环化反应,Ⅶ的环化产物的结构简式__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X的最低负价与Y的最高正价代数和为零,下列说法正确的是
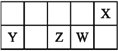
A. 原子半径的大小顺序:r(Y)>r(Z)>r(W)>r(X)
B. Z的最高价氧化物对应水化物的酸性比W的强
C. X的简单气态氢化物的稳定性比W的弱
D. X分别与Y、Z形成的化合物中化学键类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某模拟“人工树叶”电化学实验装置如下图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O),下列说法正确的是( ) 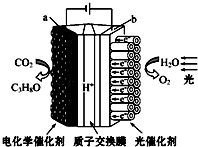
A.该装置将化学能转化为光能和电能
B.a电极的反应为:3CO2+18H+﹣18e﹣═C3H8O+5H2O
C.每生成1 mol O2 , 有44 g CO2被还原
D.该装置工作时H+从b极区向a极区迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】还原铁粉是化工生产及实验室中常用的还原剂。工业上以绿矾为原料制备还原铁粉的工艺如下:
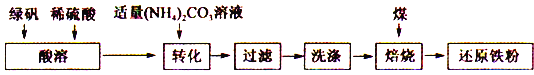
回答下列问题:
(1)酸溶过程中硫酸的作用是________________________ 。
(2)转化的目的是制得FeCO3,加液时应将(NH4)2CO3溶液加入到FeSO4中,原因是_____________。
(3)转化过程中温度不超过35℃,原因是___________________________ 。
(4)生成的FeCO3沉淀需充分洗涤,检验洗涤是否完全的方法是___________________ 。
(5)将FeCO3浊液暴露在空气中,固体表面变为红褐色,同时释放出CO2,写出该反应的化学方程式:________________________ 。
(6)在焙烧过程中需加入CaCO3进行脱硫处理。下图为加CaCO3和不加CaCO3对还原铁粉产率的影响,据图分析CaCO3的另一作用为________________________ 。
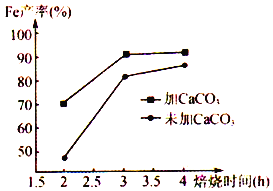
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 用醋酸除去水垢:CaCO3+2H+=Ca2++H2O+CO2↑
B. 用铜为电极电解饱和食盐水:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
C. FeBr2溶液中通入过量Cl2:2Fe2++Cl2=2Fe3++2Cl-
D. 用FeCl3溶液腐蚀印刷电路板上铜箱:2Fe3++Cu=2Fe2++Cu2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com