
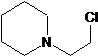 ��C��D�ķ�Ӧ����Ϊȡ����Ӧ��
��C��D�ķ�Ӧ����Ϊȡ����Ӧ��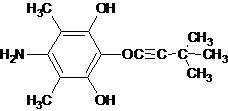 ��
�� ��
�� ��
�� Ϊԭ���Ʊ�
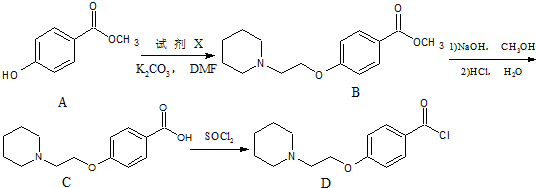
Ϊԭ���Ʊ�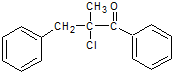 �ĺϳ�·������ͼ�����Լ����ã���
�ĺϳ�·������ͼ�����Լ����ã��� ���� ��1���ɽṹ��ʽ�ж��л��ﺬ�еĹ����ţ�
��2���Լ�X��A����ȡ����Ӧ������B��A�Ľṹ��ʽȷ��X�Ľṹ��ʽ��
��3��C��ͬ���칹�������-NH2���뱽��ֱ��������������FeCl3��Һ������ɫ��Ӧ��˵�����з��ǻ�����������4�ֲ�ͬ��ѧ�������⣬���C�IJ����Ͷȿ�֪��Ӧ��ͬ���칹�庬��C��C����
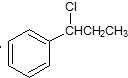
��4�� �ȷ���ȡ����Ӧ���ɴ���Ȼ����������ͪ����
�ȷ���ȡ����Ӧ���ɴ���Ȼ����������ͪ���� �����ӳɷ�Ӧ����
�����ӳɷ�Ӧ����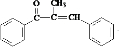 �������HCl�����ӳɷ�Ӧ������Ŀ���
�������HCl�����ӳɷ�Ӧ������Ŀ���
��� �⣺��1���ɽṹ��ʽ�ж��л��ﺬ�еĹ�����Ϊ�Ѽ����������ʴ�Ϊ���Ѽ���������
��2���Լ�X��A����ȡ����Ӧ������B��A�Ľṹ��ʽȷ��X�Ľṹ��ʽΪ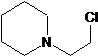
�ʴ�Ϊ��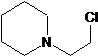
��3��C��ͬ���칹�������-NH2���뱽��ֱ��������������FeCl3��Һ������ɫ��Ӧ��˵�����з��ǻ�����������4�ֲ�ͬ��ѧ�������⣬���C�IJ����Ͷȿ�֪��Ӧ��ͬ���칹�庬��C��C��������ܵĽṹ��ʽΪ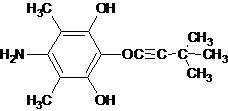

�ʴ�Ϊ��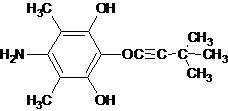

��4�� �ȷ���ȡ����Ӧ���ɴ���Ȼ����������ͪ����
�ȷ���ȡ����Ӧ���ɴ���Ȼ����������ͪ���� �����ӳɷ�Ӧ����
�����ӳɷ�Ӧ����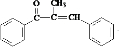 �������HCl�����ӳɷ�Ӧ������
�������HCl�����ӳɷ�Ӧ������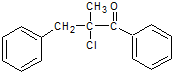 ������Ϊ
������Ϊ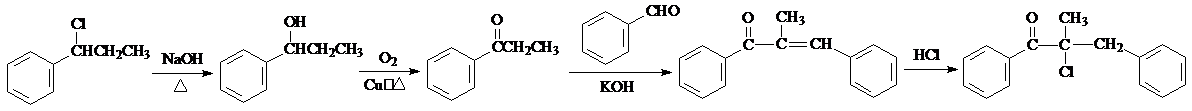
�ʴ�Ϊ��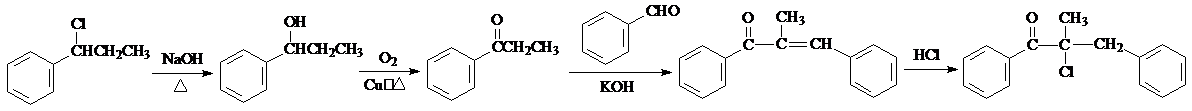
���� ���⿼���л���ĺϳɣ�Ϊ�߿��������ͣ�������ѧ���ķ��������Ŀ��飬��Ŀ�Ѷ��еȣ����ʱע����ݹ����ŵ������Լ�ת���жϣ�ע����������Ӧ������Ϊ������ؼ����״���Ϊ�л���ĺϳ����̵���ƣ�ע��֪ʶ��Ǩ�ƺ�Ӧ�ã�


 �ظ���ʦ�㲦ϵ�д�
�ظ���ʦ�㲦ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| pH | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| CuCl���� | 70 | 90 | 82 | 78 | 75 | 72 | 70 |
| ƽ��ʵ����� | 1 | 2 | 3 |
| 0.25g��Ʒ�������������Һ�������mL�� | 24.35 | 24.05 | 23.95 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
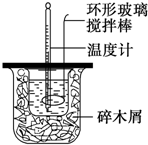 50mL 0.50mol•L-1������50mL 0.55mol•L-1NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȣ�
50mL 0.50mol•L-1������50mL 0.55mol•L-1NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ˮ�ķе㣻����ˮ�������� | |
| B�� | ˮ���ܶȣ�ˮ��ͨ������CO2����Һ��pH | |
| C�� | ˮ����������ˮ�����ĵĵ��� | |
| D�� | ˮ�����ʵ�����ˮ��Ħ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CSO�ĵ���ʽ��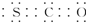 | |
| B�� | Cl-�Ľṹʾ��ͼ��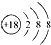 | |
| C�� | ������ӵı���ģ�ͣ� | |
| D�� | ԭ�Ӻ�����20�����ӵ���ԭ�ӣ�2017Cl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �� | B�� | �� | C�� | �� | D�� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼�������Һ�м������������������Һ��Ca2++HCO3-+OH-�TCaCO3��+H2O | |
| B�� | ����ˮ�ķ�ӦNa+2H2O=Na++2OH-+H2�� | |
| C�� | ͭƬ��ϡ���ᷴӦ��Cu+NO3-+4H+�TCu2++NO��+2H2O | |
| D�� | ��Ƭ������������Һ��Ӧ��2Al+2OH-+2H2O�T2AlO2-+3H2�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com