
【题目】结合氯气的相关知识解决下列问题。
(1)在实验室中制取Cl2,下列收集Cl2的装置中正确的是_______(填字母)。
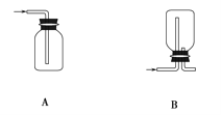
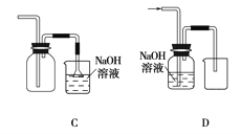
漂白粉能与盐酸发生反应,但盐酸浓度不同时,漂白粉与盐酸混合发生反应的类型不同,漂白粉与稀盐酸发生复分解反应以增强漂白性,化学方程式为_________。漂白粉与浓盐酸发生氧化还原反应会生成氯气,化学方程式为____________。
(2)图1是某同学制备氯水的装置图。
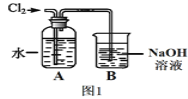
①装置B中发生反应的化学方程式为__________________。
②检验一瓶氯水是否已经完全变质,可选用的试剂是______________(填序号)。
A.硝酸银溶液B.酚酞溶液 C.碳酸钠溶液 D.紫色石蕊溶液
③氯水久置变质的主要反应方程式表示为______________________。
(3)已知氧化性:Br2>Fe3+。若在溴化亚铁溶液中通入氯气,首先被氧化的离子是_______(填离子符号)。
【答案】C Ca(ClO)2 +2HCl =CaCl2 +2HClO Ca(ClO)2+4HCl═CaCl2+2Cl2↑+2H2O Cl2+2NaOH=NaCl+NaClO+H2O D 2HClO![]() 2HCl+O2↑ Fe2+
2HCl+O2↑ Fe2+
【解析】
(1)依据氯气密度大于空气密度,可溶于水的有毒气体的物理性质选择正确的收集方法;依据强酸制备弱酸规律,盐酸与次氯酸钙反应生成氯化钙和次氯酸;
漂白粉与浓盐酸发生氧化还原反应生成氯气、氯化钙和水;
(2)①装置B中发生反应是氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;
②氯水中HClO不稳定,若变质生成盐酸,酸性增强;
(3)利用谁强谁先反应规律进行分析。
(1)A.只有进气口,没有出气口,无法排出气体,故A错误;
B. 此装置是用来收集比空气轻的气体,若收集氯气,应选择向上排空气法,需要短进长出,故B错误;
C. 装置长进短出可以收集比空气重的气体氯气,剩余的氯气有毒需要用氢氧化钠溶液吸收,为防止倒吸,用倒扣在水面的漏斗,符合要求,故C正确;
D. 氯气通入NaOH溶液会发生反应。氯气被氢氧化钠吸收,不能收集到氯气,故D错误;
故选:C;
盐酸与次氯酸钙反应生成氯化钙和次氯酸,反应的化学方程式:Ca(ClO)2 +2HCl =CaCl2 +2HClO;
漂白粉与浓盐酸发生氧化还原反应生成氯气、氯化钙和水,化学方程式:Ca(ClO)2+4HCl═CaCl2+2Cl2↑+2H2O;
故答案为:Ca(ClO)2 +2HCl =CaCl2 +2HClO;Ca(ClO)2+4HCl═CaCl2+2Cl2↑+2H2O;
(2)①装置B中发生反应的离子方程式为:Cl2+2NaOH=NaCl+NaClO+H2O,
故答案为:Cl2+2NaOH=NaCl+NaClO+H2O;
②氯水中HClO不稳定,若变质生成盐酸,酸性增强,可选紫色石蕊检验,
A. 硝酸银溶液和氯离子生成白色沉淀,不能检验一瓶氯水是否已经完全变质,故A错误;
B. 酚酞溶液在酸溶液中不变色,故B错误;
C. 碳酸钠溶液和盐酸反应生成二氧化碳气体,不能检验一瓶氯水是否已经完全变质,故C错误;
D.紫色石蕊溶液遇到酸溶液显红色,不褪色说明变质,先变红后褪色证明为变质,能检验一瓶氯水是否已经完全变质,故D正确;
故答案为:D;
③氯水久置变质会生成氯化氢和氧气,故化学方程式是2HClO![]() 2HCl+O2↑
2HCl+O2↑
故答案为:2HClO![]() 2HCl+O2↑;
2HCl+O2↑;
(3)氧化性:Br2>Fe3+,氧化性越强对应离子的还原性越弱,所以还原性:Br-<Fe2+,不同还原剂遇到同一种氧化剂时,还原性强的先反应,溴化亚铁溶液中通入氯气,首先被氧化的离子是Fe2+,
故答案为:Fe2+。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】二元化合物X呈黑棕色晶体,易潮解,易溶于水、乙醇和乙醚;熔点306℃,沸点315℃,400℃时存在二聚体。将X加热到200℃以上释放出一种单质气体:取1.2000 g X,加热完全分解为晶体B和气体C;气体C用足量KI溶液吸收,再用0.2500 mol/L Na2S2O3溶液进行滴定,消耗29.59 mL;晶体B可溶于水,所得溶液用0.0500 mol/L的K2Cr2O7溶液进行滴定,消耗24.66 mL。设分解反应转移电子数为n,则X的摩尔质量为___________;满足条件的X是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等物质的量的N2、O2、CO2混合气体通过一定量Na2O2后,体积变为原体积的8/9(同温同压),这时混合气体中N2、O2、CO2物质的量之比为( )
A. 6: 7: 3 B. 3: 3: 2
C. 3: 4: 1 D. 6: 9: 0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠常作漂白剂、杀菌剂、消毒剂。过氧化钠保存不当容易吸收空气中CO2而变质。
(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入__________溶液,充分振荡后有白色沉淀,证明Na2O2已经变质。
(2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取a g样品,并设计用下图装置来测定过氧化钠的质量分数。

①A中发生反应离子方程式为_____________________。
②将仪器连接好以后,必须进行的第一步操作是_____________________。
③B装置出来的气体是否需要干燥_________________。(填“是”或“否”)
④写出装置C中发生的所有反应的化学方程式_____________,______________。
⑤D中NaOH溶液的作用_______________________。
⑥实验结束时,读取实验中生成气体的体积时,不合理的是_______________。
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中水的体积
⑦读出量筒内水的体积后,折算成标准状况下氧气的体积为V mL,则样品中过氧化钠的质量分数为__________________。
⑧实验完成后E到F之间导管内残留水的体积会使测量结果__________。(填“偏大”、“偏小”或“不影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中,溶质的物质的量浓度为1 mol·L1的是( )
A.1 mol HCl溶于1 L 水所得的溶液
B.200 mL 5 mol·L1的NaNO3溶液稀释成1L的溶液
C.6.2 g Na2O溶于水配成100mL的溶液
D.K+物质的量浓度为1mol·L1的K2SO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校课外小组为测定某碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,甲、乙两组同学分别进行了下列相关实验。
方案Ⅰ.甲组同学用气体体积测量法
(1)把一定量样品与足量稀硫酸反应后,用如图装置测量产生CO2气体的体积,B溶液最好采用__________(以下选项中选择)使测量误差较小.

A.饱和碳酸钠溶液
B.饱和碳酸氢钠溶液
C.饱和氢氧化钠溶液
D.饱和盐酸溶液
方案Ⅱ:乙组同学的主要实验流程图如下:
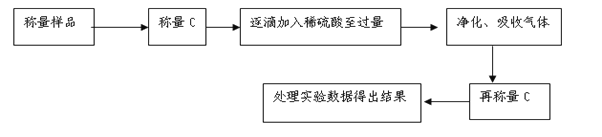
按如下图所示装置进行实验:(已知:碱石灰中含有NaOH和CaO,能吸收水分和酸性气体)
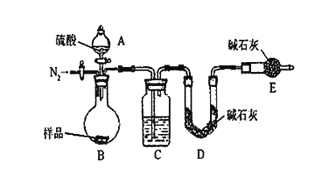
(2)在D中装碱石灰来吸收净化后的气体.E装置的作用是______________________.
(3)有的同学认为为了减少实验误差,在反应前后都通入N2,反应后通入N2的目的是_______________________________.
方案Ⅲ:丙组同学用质量法,按如下图所示的实验流程进行实验:

(4)实验时,蒸发结晶操作中,除了酒精灯外,还要用到的玻璃仪器是________
(5)有同学认为“加入适量盐酸”不好操控,应改为“过量盐酸”,便于操作且不影响测定的准确性,为什么__________________________________
(6)若实验中测得样品质量为46.4g,固体质量为40.95g,则碳酸钠的质量分数为_____.(保留3位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.向FeCl2溶液中通入Cl2:Fe2+Cl2═Fe3++2C1-
B.醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+═Ca2++H2O+CO2
C.向小苏打溶液中滴加盐酸;CO32-+2H+═H2O+CO2
D.向NH4Cl溶液中滴入烧碱溶液并加热:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列反应中,HCl作氧化剂的是( )
A.NaOH+HCl=NaCl+H2O
B.Zn+2HCl=ZnCl2+H2↑
C.MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
D.CuO+2HCl=CuCl2+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M表示摩尔质量,NA表示阿伏加德罗常数,Vm表示气体摩尔体积,ω表示溶质的质量分数,ρ(单位为gcm-3)表示溶液的密度。下列说法中不正确的是( )
A.根据摩尔质量和阿伏加德罗常数可以计算得出某气体分子的质量:![]()
B.根据气体摩尔体积和阿伏加德罗常数可以计算得出该条件下某气体分子的大小:![]()
C.根据摩尔质量和气体摩尔体积可以计算得出该条件下某气体的密度:![]()
D.根据溶质的质量分数、摩尔质量和溶液的密度可以计算出某溶液的物质的量浓度:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com