
����Ŀ��������̼�IJ����������������ҹ���Դ�����һ����Ҫս�Է���չ��һ����Ҫ�����˲�ҵ��
��1����֪��CH4��CO��H2��ȼ���ȷֱ�Ϊ890kJmol��1��283kJmol��1��285.8kJmol��1���������з�Ӧ�ķ�Ӧ�ȡ�CO2��g��+CH4��g����2CO��g��+ 2H2��g����H��___________kJmol��1��
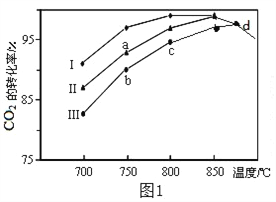
��2�����÷����е�CO2Ϊԭ����ȡ�״�����Ӧ����ʽΪ��CO2��3H2![]() CH3OH��H2O����������ͬ���ü״��ϳɷ�Ӧ�ڲ�ͬ�������������·�Ӧ��ͬʱ���CO2��ת�����淴Ӧ�¶ȵı仯��ͼ����ʾ��
CH3OH��H2O����������ͬ���ü״��ϳɷ�Ӧ�ڲ�ͬ�������������·�Ӧ��ͬʱ���CO2��ת�����淴Ӧ�¶ȵı仯��ͼ����ʾ��
�ٸ÷�Ӧ�Ħ�H_____0�������������
��d�㲻ͬ��������������CO2��ת������ͬ��ԭ����________��
 ��
�� 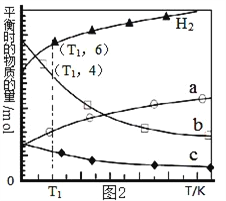
��3���ö�����̼���������ϳɵ�̼ϩ������ʼʱ��0.1MPa��n��H2����n��CO2��=3��1��Ͷ�ϱȳ��뷴Ӧ���У�������Ӧ��2CO2��g��+6H2��g��![]() C2H4��g��+4H2O��g����H����ͬ�¶���ƽ��ʱ��������̬���ʵ����ʵ�����ͼ2��ʾ��
C2H4��g��+4H2O��g����H����ͬ�¶���ƽ��ʱ��������̬���ʵ����ʵ�����ͼ2��ʾ��
�ٸ÷�Ӧ��_________�Է����У�����¡����¡�����
��b������������______________��
��T1�¶��µ�ƽ��ת����Ϊ_________________���������ʼ״̬��ƽ��ʱ�����ƽ������������İٷ���Ϊ______________��������λ��Ч���֣���
���𰸡� +247.6 �� ���ﵽƽ��״̬��������Ӱ��ƽ��ת���� ���� H2O 50% 23.1%
����������1������CH4��H2����CO��ȼ���ȷֱ�д��ȼ�յ��Ȼ�ѧ����ʽ��
��O2��g��+2H2��g��=2H2O��l����H=-571.6kJmol -1��
��CH4��g��+2O2��g��=CO2��g��+2H2O��l����H=-890kJmol-1��
��2CO��g��+O2��g��=2CO2��g����H=-566 kJmol-1��
���ø�˹���ɽ���-��-�ۿɵã� CO2��g��+CH4��g����2CO��g��+ 2H2��g����H��+247.6 kJmol��1��
��2����ͼ����֪���ü״��ϳɷ�Ӧ�ڲ�ͬ���������������������·�Ӧ��ͬʱ���CO2��ת�������ŷ�Ӧ�¶ȵ�������������С��˵������Ӧ�ﵽƽ��״̬�������¶Ȼ�ѧƽ�����淴Ӧ�����ƶ������Ը÷�ӦΪ���ȷ�Ӧ���ٸ÷�Ӧ����H ��0.��d�㲻ͬ����������������������CO2��ת������ͬ��ԭ�����ڴ��¶��¸÷�Ӧ���ﵽƽ��״̬��������Ӱ��ƽ��ת���ʡ�
��3����ͼ2��֪����Ӧ����������ƽ�������¶����߶����������Ը÷�ӦΪ���ȷ�Ӧ���������ߵı仯���ƣ������жϳ�a��b��c�������߷ֱ��ʾ������̼��ˮ����ϩ���ٸ÷�Ӧ��H<0����S<0��ֻ���ڵ����²��ܱ�֤��H-T��S<0�����Ը÷�Ӧ�ڵ����Է����С����ۺϷ�Ӧ�и���ֵĻ�ѧ�����������ߵı仯���ƽ��з����������жϳ�b������������H2O������ʼʱ��0.1MPa��n��H2����n��CO2��=3��1��Ͷ�ϱȳ��뷴Ӧ���У�������Ӧ��2CO2��g��+6H2��g��![]() C2H4��g��+4H2O��g����Ͷ�ϱ��뻯ѧ������֮����ͬ���������ַ�Ӧ���ƽ��ת��������ͬ�ġ���ͼ2��֪��T1�¶��£�������ˮ��ƽ�����ֱ�Ϊ6mol��4mol��˵�������ı仯��Ҳ��6mol�����Ը÷�Ӧ��ƽ��ת����Ϊ50%.����ʼ״̬�������Ͷ�����̼�����ʵ����ֱ�Ϊ12mol��4mol����Ӧ���ƽ����Է�������Ϊ
C2H4��g��+4H2O��g����Ͷ�ϱ��뻯ѧ������֮����ͬ���������ַ�Ӧ���ƽ��ת��������ͬ�ġ���ͼ2��֪��T1�¶��£�������ˮ��ƽ�����ֱ�Ϊ6mol��4mol��˵�������ı仯��Ҳ��6mol�����Ը÷�Ӧ��ƽ��ת����Ϊ50%.����ʼ״̬�������Ͷ�����̼�����ʵ����ֱ�Ϊ12mol��4mol����Ӧ���ƽ����Է�������Ϊ![]() ����ƽ��״̬ʱ��CO2��H2��C2H4��H2O�����ʵ����ֱ�Ϊ2mol��6mol��1mol��4mol��ƽ��ʱ�����ƽ����Է�������Ϊ
����ƽ��״̬ʱ��CO2��H2��C2H4��H2O�����ʵ����ֱ�Ϊ2mol��6mol��1mol��4mol��ƽ��ʱ�����ƽ����Է�������Ϊ![]() ���������ʼ״̬��ƽ��ʱ�����ƽ������������İٷ���Ϊ
���������ʼ״̬��ƽ��ʱ�����ƽ������������İٷ���Ϊ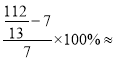 23.1% ��
23.1% ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������£�����������Һ��
�� 0.1mol/L NH4Cl
�� 0.1mol/L CH3COONH4
�� 0.1mol/L NH4HSO4
�� 0.1mol/L NH3��H2O��0.1mol/L NH4Cl�Ļ��Һ
�����Ҫ����д���пհף�
��1����Һ�ٳ����ԣ���ԭ����__________________________________(�����ӷ���ʽ��ʾ)
��2���Ƚ���Һ��������c(NH4+)�Ĵ�С��ϵ�Ǣ�____��(����������=����������)��
��3������Һ���У�_________���ӵ�Ũ��Ϊ0��1mol/L��NH3��H2O�� ___________���ӵ�Ũ��֮��Ϊ0��2 mol/L��
��4�������£������Һ�ڵ�pH=7�� CH3COO-��NH4+Ũ�ȵĴ�С��ϵ�ǣ�c(CH3COO-)______c(NH4+)(����������=����������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(SO2Cl2)�������л���ѧ���Ȼ�������ҩ���Ⱦ�ϵ���ȡ��Ҳ����Ҫ���á�ij��ѧѧϰС�����ø����Cl2��SO2�ڻ���̿������ȡ�����ȡ���Ӧ�Ļ�ѧ����ʽΪ��SO2(g)+ Cl2(g) =SO2Cl2(l) ��H =97.3 kJ��mol1��ʵ��װ����ͼ��ʾ(���ּг�װ��δ����)��
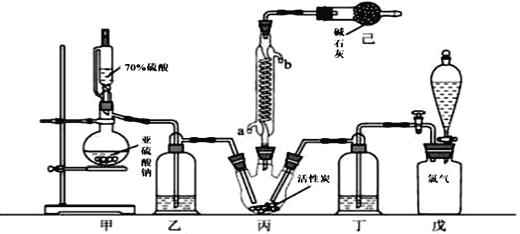
��֪��������ͨ��������Ϊ��ɫҺ�壬�۵�54.1�����е�69.1�����ڳ�ʪ����������������100��C���Ͽ�ʼ�ֽ⣬���ɶ�����������������ڷ���Ҳ�ᷢ���ֽ⡣
�ش��������⣺
��1��װ�ü�����Ϊ��Ӧ����������������Ϊ________��װ�ü���������________����ο������ַ�Ӧ�������ȣ�________��
��2��װ�����Ϸ���Һ©�������ѡ�������Լ�����_______��(ѡ����ĸ)��
A������ˮ B������ʳ��ˮ C��Ũ����������Һ D��6.0 molL1����
��3����ȱ��װ���ҺͶ�(��ʢ��Ũ����)����ʪ�����Ͷ�����������Ӧ�Ļ�ѧ����ʽ��________________________________________��
��4���Ȼ���(ClSO3H)���ȷֽ⣬Ҳ���Ƶ������ȣ�2ClSO3H ��SO2Cl2 + H2SO4���������ֲ���ķ�������_______�� (ѡ����ĸ)��
A���ؽᾧ B������ C������ D����ȡ
��5�����ڴ���������Ȼᷢ�ƣ����ܵ�ԭ����________ (�û�ѧ����ʽ�ͱ�Ҫ�����ּ��Խ���)��
��6������Ӧ�����ĵ��������Ϊ896 mL(��״����)����������ᴿ�õ�4.05 g�����������ȣ��������ȵIJ���Ϊ________��Ϊ��߱�ʵ���������ȵIJ��ʣ���ʵ���������Ҫע���������________________ ________________________________________ (д��������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ϡ����Ϊ����ʵ�Cu-Znԭ��أ�����˵������ȷ����
A.ͭΪ����B.������ͭ�����ߵ�п
C.п����������ӦD.�������������п�缫
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ѵﻯѧƽ������з�Ӧ:2X(g)+Y(g) ![]() 2Z(g)��H>0;�����¶ȵ�ͬʱ��Сѹǿ,�Է�Ӧ������Ӱ����
2Z(g)��H>0;�����¶ȵ�ͬʱ��Сѹǿ,�Է�Ӧ������Ӱ����
A. �淴Ӧ��������,����Ӧ���ʼ�С,ƽ�����淴Ӧ�����ƶ�
B. �淴Ӧ���ʼ�С,����Ӧ��������,ƽ��������Ӧ�����ƶ�
C. �����淴Ӧ���ʶ���С,ƽ�����淴Ӧ�����ƶ�
D. �����淴Ӧ���ʶ���С,ƽ��������Ӧ�����ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ϊ2 L�Ĺ̶��ܱ�������ͨ��3 mol X���壬��һ���¶��·������·�Ӧ��2X(g)![]() Y(g)��3Z(g)��
Y(g)��3Z(g)��
��1����5 min��Ӧ�ﵽƽ�⣬��ʱ��������ڵ�ѹǿΪ��ʼʱ��1.2��������Y��ʾ������Ϊ________ mol��L��1��min��1��
��2����������Ӧ�ڼס��ҡ��������ĸ�ͬ�����ܱ������н��У���ͬһ��ʱ���ڲ�������ڵķ�Ӧ���ʷֱ�Ϊ �ף�v(X)��3.5 mol��L��1��min��1�� �ң�v(Y)��2 mol��L��1��min��1������v(Z)��4.5 mol��L��1��min��1�� ����v(X)��0.075 mol��L��1��s��1��������������ͬ���¶Ȳ�ͬ�����¶��ɸߵ��͵�˳����(�����)________��

��3������ﵽ(1)��ƽ����ϵ�г��뺤������ƽ��______(����������������������������)�ƶ������Ӵﵽ(1)��ƽ����ϵ�����߲���Y���壬��ƽ��________(����������������������������)�ƶ���
��4��������ͬ��������ﵽ(1)������ƽ����ϵ���ٳ���0.5 mol X���壬��ƽ���X��ת������(1)��ƽ����X��ת������Ƚ�________��
A����ȷ�� B��ǰ��һ�����ں��� C��ǰ��һ�����ں��� D��ǰ��һ��С�ں���
��5���������¶Ⱥ�ѹǿ���䣬��ʼʱ����X��Y��Z���ʵ����ֱ�Ϊa mol��b mol��c mol���ﵽƽ��ʱ����(1)��ƽ���Ч����a��b��cӦ������Ĺ�ϵΪ_____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���У��������ִ���ը����ѧ���۵��ǣ� ��
A���������ڵ����浮����һ�δ�ը
B���������ڲ��ϵغϳ���Ȼ����û�е���Ԫ��
C���⡢�������Ԫ������������ȻԪ��֮ĸ
D�����������ԭ���У���������Ԫ�ص�ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������1molC3H8�������·�Ӧ����C3H8��C2H4+CH4��C3H8��C3H6+H2���C3H8��ת����Ϊ80%���һ��������m(CH4)=m(H2),������˵����ȷ���ǣ� ��
A. ��Ӧ���������ƽ����Է�������Ϊ35.2
B. ����ϩ�����ʵ���֮�ȣ���n(C2H4)/n(C3H6)Ϊ1��1
C. ���������ͨ��������Ȼ�̼��Һ����Һ����128g
D. ����ϩ�����ʵ���֮�ͣ���n(C2H4)+n(C3H6)Ϊ0.8mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ı�����һ��������ͨ�������ӵİٷ�������߷�Ӧ���ʵ��ǣ�������
A. �Ӵ��� B. ���� C. ��ѹ D. �Ӵ�Ӧ��Ũ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com