
|
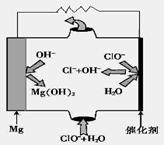
 2MgO+SO2+CO2+SO3。②根据图示可以看出反应物为Mg、ClO-和H2O,产物是Cl-和Mg(OH)2,所以反应方程式为Mg+ClO-+H2O=Cl-+Mg(OH)2。
2MgO+SO2+CO2+SO3。②根据图示可以看出反应物为Mg、ClO-和H2O,产物是Cl-和Mg(OH)2,所以反应方程式为Mg+ClO-+H2O=Cl-+Mg(OH)2。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:填空题
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.250 | 0.012 |
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1molCO 2molH2 | 1molCH3OH | 2molCH3OH | |
| 平衡数据 | CH3OH的浓度(mol/L) | c 1 | c 2 | c 3 |
| 反应的能量变化的绝对值(kJ) | a | b | c | |
| 体系压强(Pa) | P1 | P2 | P3 | |
| 反应物转化率 | α1 | α2 | α3 | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
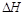 =______________。
=______________。 查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2的燃烧热为241.8 kJ·mol-1 |
| B.2H2(g)+O2(g)===2H2O(g)ΔH=-483.6 kJ·mol-1 |
| C.1 mol H2完全燃烧生成液态水放出的热量大于241.8 kJ |
| D.断裂1 mol H2O的化学键吸收的总能量大于断裂1 mol H2和0.5 mol O2的化学键所吸收的总能量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g)△H=-92.0KJ·mol-1,将1mol N2和3mol H2充入一密闭容器中,保持恒温恒压,在催化剂存在时进行反应,达到平衡时,测得N2的转化率为20%。若在相同条件下,起始时在该容器中充入2mol NH3,反应达到平衡时的热量变化是
2NH3(g)△H=-92.0KJ·mol-1,将1mol N2和3mol H2充入一密闭容器中,保持恒温恒压,在催化剂存在时进行反应,达到平衡时,测得N2的转化率为20%。若在相同条件下,起始时在该容器中充入2mol NH3,反应达到平衡时的热量变化是| A.吸收18.4KJ热量 | B.放出73.6KJ热量 |
| C.放出18.4KJ热量 | D.吸收73.6KJ热量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Q1-3Q2+Q3 | B.3Q1-Q2+Q3 | C.Q1+Q2+Q3 | D.2(Q1+Q2+Q3) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.N2H4(g)+NO2(g)===3/2N2(g)+2H2O(g) ΔH=+567.85kJ·mol-1 |
| B.N2H4(g)+NO2(g)===3/2N2(g)+2H2O(g) ΔH=-567.85kJ·mol-1 |
| C.N2H4(g)+NO2(g)===3/2N2(g)+2H2O(l) ΔH=+567.85kJ·mol-1 |
| D.N2H4(g)+NO2(g)===3/2N2(g)+2H2O(l) ΔH=-567.85kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com