
ŅŃÖŖ£ŗCO2+3H2O+2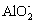 ØTØT2Al(OH)3”ż+CO
ØTØT2Al(OH)3”ż+CO![]()
£Ø1£©ÕāĪåÖÖČÜŅŗµÄpHÓÉŠ”µ½“óµÄĖ³ŠņŹĒ£ŗ________£ØĢī±ąŗÅ£©”£?
£Ø2£©½«ĪåÖÖČÜŅŗĻ”ŹĶĻąĶ¬µÄ±¶ŹżŹ±£¬ĘäpH±ä»Æ×ī“óµÄŹĒ£ŗ________£ØĢī±ąŗÅ£©”£?
£Ø3£©ŌŚÉĻŹöĪåÖÖČÜŅŗÖŠ·Ö±š¼ÓČėAlCl3ČÜŅŗ£¬ÄܲśÉśĪŽÉ«ĪŽĪ¶ĘųĢåµÄŹĒ£ŗ________£ØĢī±ąŗÅ£©”£
£Ø4£©½«ÉĻŹö¢Ł¢Ś¢Ū¢ÜĖÄÖÖČÜŅŗĮ½Į½»ģŗĻŹ±£¬ÓŠŅ»¶ŌČÜŅŗĻą»„¼äÄÜ·¢Éś·“Ó¦£¬Š“³öøĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ”””””””””””””””””””””””””””””””””””£?
£Ø1£©¢Ü¢Ś¢Ł¢Ū¢Ż?
£Ø2£©¢Ż””£Ø3£©¢Ł¢Ś?
£Ø4£©HCO![]() +
+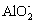 +H2OØTØTAl(OH)3”ż+CO
+H2OØTØTAl(OH)3”ż+CO![]()
½āĪö£ŗ±¾ĢāÖøĆ÷¢ŁÅضČĻąĶ¬0.1 mol”¤L -1 ¢ŚCO2+2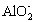 +3H2OØTØT2Al(OH)3”ż+CO
+3H2OØTØT2Al(OH)3”ż+CO![]()
£Ø1£©ĖįŠŌŌ½Čõ£¬ĘäŃĪĖ®½ā³Ģ¶ČŌ½“ó£¬pHŌ½“ó”£ŌņpHÓÉŠ”µ½“óµÄĖ³ŠņŹĒ¢Ü¢Ś¢Ł¢Ū¢Ż£¬CH3COONa£¼NaHCO3£¼Na2CO3£¼NaAlO2£¼NaOH?
ĻąĶ¬µÄ¶ąŌŖČõĖį£¬ĘäĖįŹ½ŃĪµÄĖ®½ā³Ģ¶ČŠ”ÓŚÕżŃĪµÄĖ®½ā³Ģ¶Č”£?
£Ø2£©Ļ”ŹĶĻąĶ¬µÄ±¶Źż£¬ŌņNaOHµÄpH±ä»Æ×ī“ó£¬ŅņĪŖNaOHĶźČ«µēĄė”£?
£Ø3£©ÓėAlCl3·“Ó¦µÄÓŠ¢Ł¢Ś¢Ū¢Ż£¬µ«ÄܲśÉśĘųĢåµÄŹĒ¢Ł¢Ś”£
2Al3++3CO![]() +3H2O2ØTØTAl(OH)3”ż+3CO2”ü??
+3H2O2ØTØTAl(OH)3”ż+3CO2”ü??
Al3++3HCO![]() ØTØTAl(OH)3”ż+3CO2”ü?
ØTØTAl(OH)3”ż+3CO2”ü?
Al3++3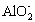 +6H2OØTØT4Al(OH)3”ż?
+6H2OØTØT4Al(OH)3”ż?
£Ø4£©Į½Į½»ģŗĻÄÜ·“Ó¦µÄŹĒNaHCO3ŗĶNaAlO2”£?
HCO![]() +
+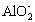 +H2OØTØTAl(OH)3”ż+CO
+H2OØTØTAl(OH)3”ż+CO![]()


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢·“Ó¦ĪĀ¶Č10”ć£¬Na2S2O3Ģå»ż5ml£¬ÅضČ0.2/mol?L-1£¬H2SO4Ģå»ż5ml£¬ÅضČ0.1/mol?L-1£¬H2OĢå»ż10mL | B”¢·“Ó¦ĪĀ¶Č10”ć£¬Na2S2O3Ģå»ż5ml£¬ÅضČ0.1/mol?L-1£¬H2SO4Ģå»ż5ml£¬ÅضČ0.1/mol?L-1£¬H2OĢå»ż10mL | C”¢·“Ó¦ĪĀ¶Č30”ć£¬Na2S2O3Ģå»ż5ml£¬ÅضČ0.1/mol?L-1£¬H2SO4Ģå»ż5ml£¬ÅضČ0.1/mol?L-1£¬H2OĢå»ż10mL | D”¢·“Ó¦ĪĀ¶Č30”ć£¬Na2S2O3Ģå»ż5ml£¬ÅضČ0.2/mol?L-1£¬H2SO4Ģå»ż5ml£¬ÅضČ0.2/mol?L-1£¬H2OĢå»ż10mL |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŃÖŖ£ŗCO2+3H2O+2![]() ====2Al(OH)3”ż+
====2Al(OH)3”ż+![]()
£Ø1£©ÕāĪåÖÖČÜŅŗµÄpHÓÉŠ”µ½“óµÄĖ³ŠņŹĒ_______________£ØĢī±ąŗÅ£©”£
£Ø2£©½«ĪåÖÖČÜŅŗĻ”ŹĶĻąĶ¬µÄ±¶ŹżŹ±£¬ĘäpH±ä»Æ×ī“óµÄŹĒ_______________£ØĢī±ąŗÅ£©”£
£Ø3£©ŌŚÉĻŹöĪåÖÖČÜŅŗÖŠ·Ö±š¼ÓČėAlCl3ČÜŅŗ£¬ÄܲśÉśĪŽÉ«ĪŽĪ¶ĘųĢåµÄŹĒ_______£ØĢī±ąŗÅ£©”£
£Ø4£©½«ÉĻŹö¢Ł¢Ś¢Ū¢ÜĖÄÖÖČÜŅŗĮ½Į½»ģŗĻŹ±£¬ÓŠŅ»¶ŌČÜŅŗĻą»„¼äÄÜ·¢Éś·“Ó¦£¬Š“³öøĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ__________________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻÖÓŠÅضČ0.1 mol”¤L-1µÄĪåÖÖµē½āÖŹČÜŅŗ¢ŁNA2CO3 ¢ŚNAHCO3 ¢ŪNAAlO2 ¢ÜCH3COONA ¢ŻNAOH
ŅŃÖŖ£ŗCO2+3H2O+2![]() ====2Al(OH)3”ż+
====2Al(OH)3”ż+![]()
£Ø1£©ÕāĪåÖÖČÜŅŗµÄpHÓÉŠ”µ½“óµÄĖ³ŠņŹĒ_______________£ØĢī±ąŗÅ£©”£
£Ø2£©½«ĪåÖÖČÜŅŗĻ”ŹĶĻąĶ¬µÄ±¶ŹżŹ±£¬ĘäpH±ä»Æ×ī“óµÄŹĒ_______________£ØĢī±ąŗÅ£©”£
£Ø3£©ŌŚÉĻŹöĪåÖÖČÜŅŗÖŠ·Ö±š¼ÓČėAlCl3ČÜŅŗ£¬ÄܲśÉśĪŽÉ«ĪŽĪ¶ĘųĢåµÄŹĒ_______£ØĢī±ąŗÅ£©”£
£Ø4£©½«ÉĻŹö¢Ł¢Ś¢Ū¢ÜĖÄÖÖČÜŅŗĮ½Į½»ģŗĻŹ±£¬ÓŠŅ»¶ŌČÜŅŗĻą»„¼äÄÜ·¢Éś·“Ó¦£¬Š“³öøĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ
_____________________________________________________________________ӣ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2011-2012ѧğÕć½Ź”¼ĪŠĖŅ»ÖŠøßŅ»10ŌĀ·ŻŌĀæ¼»ÆѧŹŌ¾ķ ĢāŠĶ£ŗŹµŃéĢā
ŹµŃéŹŅŠčŅŖ0.1 mol/L NaOHČÜŅŗ450 mLŗĶ0.5 mol/LĮņĖįČÜŅŗ450 mL.øł¾ŻÕāĮ½ÖÖČÜŅŗµÄÅäÖĘĒéæö»Ų“šĻĀĮŠĪŹĢā£ŗ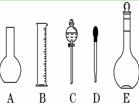
(1)ČēĶ¼ ĖłŹ¾µÄŅĒĘ÷ÖŠÅäÖĘČÜŅŗæĻ¶Ø²»ŠčŅŖµÄŹĒ”””” (ĢīŠņŗÅ)£¬
ĖłŹ¾µÄŅĒĘ÷ÖŠÅäÖĘČÜŅŗæĻ¶Ø²»ŠčŅŖµÄŹĒ”””” (ĢīŠņŗÅ)£¬
ŅĒĘ÷CµÄĆū³ĘŹĒ £¬
±¾ŹµŃéĖłŠč²£Į§ŅĒĘ÷E¹ęøńĪŖ”””””””” mL”£
(2)ĻĀĮŠ²Ł×÷ÖŠ£¬ČŻĮæĘæĖł²»¾ß±øµÄ¹¦ÄÜÓŠ””””””””””(ĢīŠņŗÅ)”£
A£®ÅäÖĘŅ»¶ØĢå»ż×¼Č·ÅضČ µÄ±ź×¼ČÜŅŗ µÄ±ź×¼ČÜŅŗ | B£®³¤ĘŚÖü“ęČÜŅŗ |
| C£®ÓĆĄ“¼ÓČČČܽā¹ĢĢåČÜÖŹ | D£®ĮæČ”Ņ»¶ØĢå»żµÄŅŗĢå |
 ĮōŅ»Ī»Š”Źż)”£Čē¹ūŹµŃéŹŅÓŠ10 mL”¢25mL”¢50 mLĮæĶ²£¬Ó¦Ń”ÓĆ”””””” mL¹ęøńµÄĮæĶ²×īŗĆ”£
ĮōŅ»Ī»Š”Źż)”£Čē¹ūŹµŃéŹŅÓŠ10 mL”¢25mL”¢50 mLĮæĶ²£¬Ó¦Ń”ÓĆ”””””” mL¹ęøńµÄĮæĶ²×īŗĆ”£²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com