
| A. | HCO3-一定不能大量存在 | B. | pH一定是12 | ||
| C. | 加入铝片一定能产生氢气 | D. | 一定不是NH4Cl溶液 |
分析 根据水电离出的c(H+)=1×10-12 mol/L,水的电离受到抑制,该溶液可能为酸或碱或盐的溶液;
A.根据离子之间结合生成水、气体、沉淀,等,则离子不能大量共存;
B.水电离出的c(H+)=1×10-12 mol/L,溶液也可为强酸溶液;
C.该溶液的溶质可能为强氧化性酸;
D.该溶液的溶质可能为盐溶液,但一定不是水解的盐;
解答 解:A.水电离出的c(H+)=1×10-12 mol/L,该溶液可能为酸或碱的溶液,当溶液为碱性时:HCO3-+OH-═CO32-+H2O,当溶液为酸性时:H++HCO3-=H2O+CO2↑,所以在该溶液中一定不能大量共存,故A正确;
B.当该溶液为pH=2的盐酸溶液,水电离出的c(H+)也为1×10-12 mol/L,故B错误;
C.可能是pH=2的HNO3这样的强氧化性酸,加入铝片后,一定不能生成氢气,故C错误;
D.可能是pH=2的NaHSO4这样的盐溶液,但一定不是NH4Cl溶液,因为氯化铵溶液中铵根离子水解促进水的电离,氢离子浓度增大,故D正确;
故选AD.
点评 本题考查水电离出的氢离子浓度为1×10-12mol/L的溶液,则溶液可能为酸或碱或盐的溶液,明确由水电离出的氢离子浓度及利用该信息来分析问题是解答的关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | NH4+、Al3+、SO42-、NO3- | B. | K+、Na+、CO32-、NO3- | ||
| C. | K+、NH4+、MnO4-、SO42- | D. | Na+、K+、NO3-、HSO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
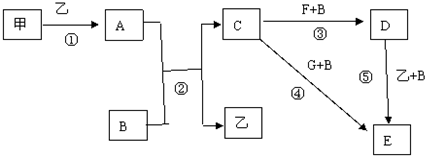
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,下列说法正确的是( )
在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,下列说法正确的是( )| A. | 外电路的电流方向为:X→外电路→Y | |
| B. | X极上发生的是还原反应 | |
| C. | 溶液中氢离子向X极移动 | |
| D. | 若两电极都是金属,则它们的活动性顺序为X>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
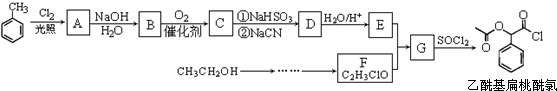
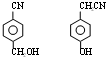
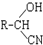 ,RCN$\stackrel{H_{2}O/H+}{→}$RCOOH,RCOOH$\stackrel{SOCl_{2}}{→}$RCOCl$\stackrel{R′OH}{→}$RCOOR′
,RCN$\stackrel{H_{2}O/H+}{→}$RCOOH,RCOOH$\stackrel{SOCl_{2}}{→}$RCOCl$\stackrel{R′OH}{→}$RCOOR′ ,E中含氧官能团的名称醇羟基和羧基.
,E中含氧官能团的名称醇羟基和羧基.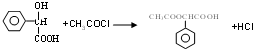 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+ | B. | Fe3+ | C. | Fe2+ | D. | H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2O有氧化性,在该反应中是氧化产物 | |
| B. | N2O会迅速与人体血红蛋白结合,使人中毒 | |
| C. | 上述反应,每消耗2molNO2,就会生成22.4LN2O | |
| D. | 在常温常压下,46gNO2参加反应转移电子3mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)瑞典化学家舍勒将软锰矿(主要成分MnO2)与浓盐酸混合加热,在世界上首先制得了氯气.写出该反应的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(1)瑞典化学家舍勒将软锰矿(主要成分MnO2)与浓盐酸混合加热,在世界上首先制得了氯气.写出该反应的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com