
(10分)Na2S2O3·5H2O可作为高效脱氯剂,工业上用硫铁矿(FeS2)为原料制备该物质的流程如下。

已知:I.气体A可以使品红溶液褪色,与硫化氢(H2S)混合能获得单质硫。
II.pH约为11的条件下,单质硫与亚硫酸盐可以共热生成硫代硫酸盐。
回答下列问题:
(1)沸腾炉中将粉碎的硫铁矿用空气吹动使之达到“沸腾”状态,其目的是_____________。
(2)吸收塔中的原料B可以选用____________(填字母序号)。
a.NaCl溶液 b.Na2CO3溶液 c.Na2SO4溶液
(3)某小组同学用下图装置模拟制备Na2S2O3的过程(加热装置已略去)。

①A中使用70%的硫酸比用98%的浓硫酸反应速率快,其原因是______。装置B的作用是_______。
②C中制备Na2S2O3发生的连续反应有:Na2S +H2O +SO2===Na2SO3 +H2S、_____和__________。
(4)工程师设计了从硫铁矿获得单质硫的工艺,将粉碎的硫铁矿用过量的稀盐酸浸取,得到单质硫和硫化氢气体,该反应的化学方程式为_________________。
(10分,未标分数的空,每空1分) (1)使固体与气体充分接触,加快反应速率 (2)b
(3)① 该反应的实质是H+与SO32-反应,70%的硫酸中含水较多,c(H+)和c(SO32-)都较大,生成SO2速率更快;防止倒吸 ② 2H2S + SO2=3S + 2H2O或2H2S + H2SO3=3S↓+ 3H2O(2分)
Na2SO3 + S Na2S2O3(2分) (4)FeS2 + 2HCl=FeCl2 + H2S↑+ S↓(2分)
Na2S2O3(2分) (4)FeS2 + 2HCl=FeCl2 + H2S↑+ S↓(2分)
【解析】
试题分析:(1)沸腾炉中将粉碎的硫铁矿用空气吹动使之达到“沸腾”状态,可以使固体与气体充分接触,从而加快反应速率。
(2)气体A可以使品红溶液褪色,说明是SO2。溶液C与S单质反应生成硫代硫酸钠,则溶液C是亚硫酸钠溶液,所以溶液B是碳酸钠吸收SO2后转化为亚硫酸钠,答案选b。
(3)① 由于该反应的实质是H+与SO32-反应,70%的硫酸中含水较多,c(H+)和c(SO32-)都较大,生成SO2速率更快,而浓硫酸中氢离子浓度小,所以A中使用70%的硫酸比用98%的浓硫酸反应速率快;SO2易溶于水,所以装置B的作用是防止倒吸。
②根据反应原理可知还必需有单质S产生,则后续的反应为2H2S + SO2=3S + 2H2O或2H2S + H2SO3=3S↓+ 3H2O,生成的S与亚硫酸钠反应生成硫代硫酸钠,方程式为Na2SO3 + S Na2S2O3。
Na2S2O3。
(4)将粉碎的硫铁矿用过量的稀盐酸浸取,得到单质硫和硫化氢气体,则根据原子守恒可知该反应中含有氯化亚铁生成,则反应的化学方程式为FeS2 + 2HCl=FeCl2 + H2S↑+ S↓。
考点:考查物质制备工艺流程图的分析与应用


科目:高中化学 来源:2014-2015学年湖南省高三上学期第三次月考化学试卷(解析版) 题型:选择题
某1 L混合溶液中,溶质X、Y的浓度都为0.1 mol·L-1,向混合溶液中滴加某溶液Z(0.1 mol· L-1氢氧化钠或硫酸溶液),所得沉淀的物质的量如图所示,则X、Y、Z分别是
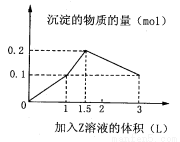
A.硫酸铝、硫酸铁、氢氧化钠
B.硫酸铝、硫酸镁、氢氧化钠
C.偏铝酸钠、氢氧化钡、硫酸
D.偏铝酸钠、氯化钡、硫酸
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省邯郸市高三上学期1月教学质量检测化学试卷(解析版) 题型:选择题
下列图示与对应的叙述相符的是




A.图甲表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化
B.图乙表示向CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b
C.图丙表示催化剂能改变化学反应的焓变
D.图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g) N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省高三上学期期末理综化学试卷(解析版) 题型:填空题
(选考)【化学——物质结构与性质】(15分)
W、Q、R、X、Y、Z六种元素的原子序数逐渐增大。已知W原子1s轨道上只有一个电子,Q、X原子p轨道的电子数分别为2和4,Z的原子序数为29,除Z外均为短周期主族元素,Y原子的价电子排布为(n+1)sn(n+1)pn。请回答下列问题:
(1)Q和W能形成一种化合物的相对分子质量为28,则该化合物的中心原子采取的杂化轨道类型是 ,该分子中含有____个 键。
键。
(2)Z原子的核外电子排布式为 ;向Z的硫酸盐中逐滴加入氨水先产生沉淀,后沉淀溶解为深蓝色溶液,加入乙醇会析出蓝色晶体,该晶体中Z的离子与NH3之间的化学键为 。
(3)这六种元素中,电负性最大与最小的两种非金属元素形成的晶体属于____晶体;W、Q、X三种元素之间可以形成多种化合物,其中邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点,理由是 。邻甲基苯甲醛分子中碳原子轨道的杂化类型为 。1 mol 苯甲醛分子中σ键为 mol。
(4)元素X的阴离子Xn-中所有电子正好充满K和L电子层,CnX晶体的最小结构单元如图所示。

该晶体中阳离子和阴离子个数比为____,晶体中每个Xn-被 个等距离的C+离子包围。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省高三上学期期末理综化学试卷(解析版) 题型:选择题
下列各组离子,一定能在指定环境中大量共存的是
A.在含有大量I-离子的溶液中:Cl?、Fe3+、Al3+、Cu2+
B.滴加石蕊试液显红色的溶液:Fe2+、NH4+、Cl-、NO3-能够大量共存
C.在由水电离出的c(H+)=10-12 mol·L-1的溶液中:Na+、Ba2+、Cl?、Br?
D.在加入Al能放出大量H2的溶液中:NH4+、SO42? 、C1?、HCO3?
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市海淀区高三上学期期末化学试卷(解析版) 题型:选择题
下述实验方案能达到实验目的的是
编号 | A | B | C | D |
实验 方案 | |
|
|
|
实验 目的 | 实验室制备乙酸乙酯 | 分离乙酸和水 | 验证溴乙烷在氢氧化钠乙醇溶液中发生消去反应产生的乙烯 | 收集乙烯并验证它与溴水发生加成反应 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市海淀区高三上学期期末化学试卷(解析版) 题型:选择题
关于0.1mol·L-1NaHCO3溶液,下列说法正确的是
A.溶质水解反应:HCO3- +H2O H3O++CO32-
H3O++CO32-
B.离子浓度关系:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-)
C.微粒浓度关系:c(Na+)>c(HCO3-) >c(H2CO3)>c(CO32-)
D.微粒浓度关系:c(Na+)=2[c(H2CO3)+c(HCO3-)+c(CO32-)]
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省名校新高考研究联盟高三上学期联考化学试卷(解析版) 题型:选择题
X、Y、Z、M、W为五种短周期元素。它们在周期表的相对位置如下表:
M | |||||||
X | Y | Z | |||||
W |
则下列说法正确的是:
A.Y、M形成的气态化合物在标准状况下的密度为0.76 g.L-1
B.原子半径:W>Z>Y>X>M
C.由X元素形成的单质一定是原子晶体
D.XZ2、X2M2、W2Z2均为直线型的共价化合物
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市崇明县高三上学期期末考试化学试卷(解析版) 题型:计算题
(本题共14分)合金的性能往往优于组成金属,因而用途非常广泛。钠钾合金可在核反应堆中用作导热剂。5.05g钠钾合金溶于200mL水生成0.075mol氢气。
54.计算溶液中氢氧根离子的物质的量浓度(忽略溶液体积变化)。
55.计算并确定该钠-钾合金的化学式。
镁铝合金广泛用于火箭、导弹和飞机制造业等。取不同质量的镁铝合金样品分别和30ml相同浓度的盐酸反应,所取合金质量与产生气体体积(标况下)如下表所示:
实验序号 | A | B | C |
合金质量/mg | 510 | 765 | 918 |
气体体积/mL | 560 | 672 | 672 |
56.计算镁铝合金中镁铝的质量之比。
铜锡合金,又称青铜,是人类使用最早的合金。不同的铜锡比例可以产生不同的效用,若含锡量为1/4—1/7(质量比)的青铜被称作重青铜,受敲击时能发出洪亮的声音。
57.现有一铜锡合金样品,可通过至少增加ag铜或至少减少bg锡恰好使其成为钟青铜,且最终得到的钟青铜质量正好相差一半。求原铜锡合金样品中铜锡的物质的量之比。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com