
| A、CH3Cl+Cl2→CH2Cl2+HCl |
| B、CH3-CH=CH2+Br2─→CH3-CHBr-CH2Br |
C、 |
D、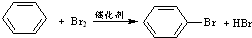 |
 ,甲苯中氢离子被氯原子取代,该反应为取代反应,故C错误;
,甲苯中氢离子被氯原子取代,该反应为取代反应,故C错误;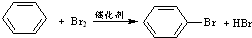 ,苯环上的氢原子被溴原子取代,该反应为取代反应,故D错误;
,苯环上的氢原子被溴原子取代,该反应为取代反应,故D错误;

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(H+) |
| c(HA) |
| c(OH-) |
| c(H+) |
| c(H+)?c(A-) |
| c(HA) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、降低温度,Y的转化率增大 |
| B、加入催化剂,Z的产率增大 |
| C、增大c(X),X的转化率增大 |
| D、减小容器体积,平衡向右移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| △ |
| A、SO2为0.4 mol/L,O2为0.2 mol/L |
| B、SO2为0.25 mol/L |
| C、SO3为0.4 mol/L |
| D、SO2、SO3均为0.15 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾[KAl(SO4)2?12H2O]在水中能形成Al(OH)3胶体,可用作净水剂 |
| B、用蒸馏水充分浸润燃尽后的火柴头,然后加入硝酸银和稀硝酸检验火柴头中氯元素 |
| C、浓H2SO4有强氧化性,常温下能与Cu发生剧烈反应 |
| D、用食醋和碘化钾淀粉试纸可以鉴别NaNO2和NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只含非极性键的分子一定是非极性分子 |
| B、含有极性键的分子一定是极性分子 |
| C、非极性分子一定含有非极性键 |
| D、由极性键构成的双原子分子一定是极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学平衡常数是一个比值,没有单位 |
| B、化学平衡常数是温度的函数,温度升高其值增大 |
| C、一个化学反应的平衡常数与物质的计量数无关 |
| D、对于同类型反应,化学平衡常数K的大小反映了化学反应可能进行的程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| L/min | 0 | 2 | 4 | 6 | 8 | … | 16 | 18 |
| n(X)/mol | 1.600 | 1.200 | 1.100 | 1.075 | … | … | 1.000 | 1.000 |
| c2(Z) |
| c(X)?c(Y) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com