
下列指定反应的离子方程式正确的是
A.Cl2通入水中:Cl2+H2O=2H++Cl-+ClO-
B.铜丝插入稀硝酸:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
C.向NaClO溶液中通入过量SO2:ClO-+SO2+H2O=HClO+HSO3-
D.向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
科目:高中化学 来源:2017届河北省高三上五调考试化学卷(解析版) 题型:选择题
下列有关实验的说法不正确的是( )
A.容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶都无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗
B.在4 mL0.1 mol/L的K2Cr2O7溶液中滴加数滴1 mol/L的NaOH溶液,溶液颜色从橙色变成黄色
C.探究化学反应的限度:取5 mL 0.1 mol/LKI溶液,滴加0.1 mol/LFeCl3溶液5~6滴,充分反应,可根据溶液中既含I2又含I-的实验事实判断该反应是可逆反应
D.将含有少量氯化钾的硝酸钾放入烧杯中,加水溶解并加热、搅拌,当溶液表面出现一层晶膜时停止加热,冷却结晶、过滤即可得到大量硝酸钾晶体
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二12月月考化学卷(解析版) 题型:选择题
配位化合物的数量巨大,组成和结构形形色色,丰富多彩。配合物[Cu(NH3)4](OH)2的中心离子、配体、中心离子的电荷数和配位数分别为
A.Cu2+、NH3、+2、4 B.Cu+、NH3、+1、4
C.Cu2+、OH-、+2、2 D.Cu2+、NH3、+2、2
答
查看答案和解析>>
科目:高中化学 来源:2017届西藏林芝一中高三上月考四化学试卷(解析版) 题型:选择题
下列仪器和装置,用橡胶管经过简单连接,可制备收集多种不同的气体(暂不考虑尾气吸收)。关于这些装置的连接,下列说法正确的是

A.制备收集Cl 2:连接a→d→f B.制备收集NO2,连接a→c→f
2:连接a→d→f B.制备收集NO2,连接a→c→f
C.制备收集H2S,连接b→c→e D.制备收集NH3,连接b→d→e
查看答案和解析>>
科目:高中化学 来源:2017届西藏拉萨中学高三上期末理综化学卷(解析版) 题型:推断题
X、Y、Z、Q、W、R六种短周期元素原子序数依次增大。化合物甲由X、Z、Q三种元素组成,常温下0.1mol/L甲溶液的pH=13。工业上常用电解饱和QR溶液生成甲;化合物乙由X、R两种元素组成。请回答下列问题:
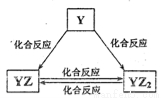
(1)Q的离子结构示意图为____________。
(2)Y元素的单质能发生如图所示的转化,请写出图中反应YZ2→YZ的化学方程式:___________(注明反应条件)。在甲溶液中通入足量YZ2气体,所得溶液呈碱性,写出该溶液中的阴离子浓度由大到小的顺序:______________。
(3)W的单质既能与甲溶液反应,又能与乙溶液反应。
①常温下,将W的单质和甲溶液混合,发生反应的离子方程式为____________;
② Q、W金属性的强弱为Q>W,下列表述中正确的且能证明这一事实的是__________(填序号)
a. Q单质的熔点比W单质的低
b. W单质的硬度比Q大
c. Q单质能将W从它的盐溶液中置换出来
d. Q的最高价氧化物的水化物的碱性比W的最高价氧化物的水化物的碱性强
查看答案和解析>>
科目:高中化学 来源:2017届江西师大附中高三12月月考化学试卷(解析版) 题型:推断题
Ⅰ、前20号主族元素A、B、C、D、E、F的原子序数依次增大,它们的原子核最外层电子数之和为18。A的原子半径为自然界最小,B、F为同一主族,E为地壳中含量最多的金属元素,F原子的最外层与最内层电子数相等。C、D可以形成两种常见化合物。试回答以下问题:
(1)写出C与F元素形成的化合物的电子式
(2)A、C、D三种元素形成的化合物C2A4D2中一定含有 。(填“离子键”、“极性共价键”或“非极性共价键”)
(3)由D、E、F形成的简单离子的离子半径由大到小的顺序是 。(用元素离子符号表示)
(4)元素B的性质与元素E的性质很相似,试写出以下反应的离子方程式:
B的氧化物与氢氧化钠溶液反应:
Ⅱ、现有A、B、C、D四种短周期元素,A分别与B、C、D结合生成甲、乙、丙三种化合物,且甲、乙、丙三分子均为10电子粒子,C、D结合生成化合物丁。有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如下图所示:

(1)根据以上条件可以确定A、B、C、D四种元素中的三种元素。不能被确定的第四种元素是________。(填写A B C D中的一种)
(2)依据下列条件可以进一步确定上述第四种元素:①甲与丙以及乙与丙均能够发生反应 ②甲、丙都是无色、有刺激性气味的物质。据此,写出C+丙―→乙+丁的化学反应方程式___________。
查看答案和解析>>
科目:高中化学 来源:2017届江西师大附中高三12月月考化学试卷(解析版) 题型:选择题
某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O 、CO2转变为H2、CO。其过程如下:
、CO2转变为H2、CO。其过程如下:
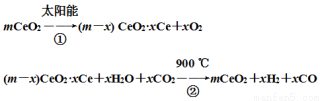
下列说法不正确的是( )
A.该过程中CeO2为H2O、CO2转变为H2、CO的催化剂
B.该过程实现了太阳能向化学能的转化
C.1molCeO2参加反应,共生成2x mol的气体
D.以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH--2e-=CO32-+2H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高二上月考二化学卷(解析版) 题型:推断题
有机物A是最常用的食用油抗氧化剂,分子式为C10H12O5,可发生如下转化:
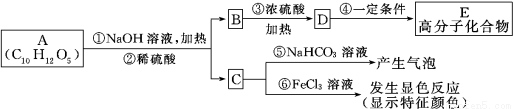
已知B的相对分子质量为60,分子中只含一个甲基。C的结构可表示为: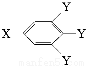 (其中:-X、—Y均为官能团)。回答下列问题:
(其中:-X、—Y均为官能团)。回答下列问题:
(1)A的结构简式为 。B的结构简式____________ 
(2)官能团—X的名称为 ,高聚物E链节为 。
(3)反应①的化学方程式为______________
(4)从分子结构上看,A具有抗氧化作用的主要原因是 (填序号)。
a.含有苯环 b.含有羰基 c.含有酚羟基
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一12月月考化学试卷(解析版) 题型:实验题
甲同学进行Fe2+还原性的实验,针对异常现象进行探究。
实验:向2 mL FeCl2溶液中滴加2滴0.1 mol•L-1 KSCN溶液,无现象;再滴加5滴5% H2O2溶液(物质的量浓度约为1.5 mol•L-1、pH约为5(酸性环境)),观察到溶液变红,大约10秒左右红色褪去,有气体生成(经检验为O2)。
(1)用离子方程式表示实验中溶液变红的原因: 、 。
(2)甲探究实验中溶液褪色的原因:
I.取褪色后溶液两份,一份滴加FeCl3溶液无现象;另一份滴加KSCN溶液出现红色;
II.取褪色后溶液,滴加盐酸和BaCl2溶液,产生白色沉淀。
III.向2 mL 0.1 mol•L-1 FeCl3溶液中滴加2滴0.1 mol•L-1 KSCN溶液,变红,通入O2,无明显变化。
① 实验I说明 ;②实验III说明 。
得出结论:溶液褪色的原因是酸性条件下H2O2将SCN-氧化成SO42-。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com