
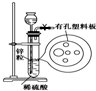
 如图为实验室制氢气的简易装置.若在加稀硫酸时发现锌粒与稀硫酸没有接触而稀硫酸不够了,为使该反应顺利进行,可以从长颈漏斗中加入的试剂是( )
如图为实验室制氢气的简易装置.若在加稀硫酸时发现锌粒与稀硫酸没有接触而稀硫酸不够了,为使该反应顺利进行,可以从长颈漏斗中加入的试剂是( )| A. | ①③⑤ | B. | ①②③ | C. | ④⑤⑥ | D. | ①②③⑤ |
分析 加入的物质应该具备以下条件:不能和容器中的物质反应生成其它气体;能够让稀硫酸和锌混合生成氢气,以此解答该题.
解答 解:①食盐水和锌和硫酸都不反应,所以不影响氢气的生成,只是降低反应速率,故正确;
②加入KNO3溶液后,相当于溶液中含有硝酸,硝酸和锌反应产生其它气体,故错误;
③适量稀硫酸铜溶液,锌能置换出铜,锌、铜和硫酸构成原电池能加快反应速率,但不产生其它气体,即不影响氢气,故正确;
④Na2CO3溶液和硫酸反应生成二氧化碳,所以能影响氢气,故错误;
⑤CCl4和硫酸、锌都不反应,所以不影响氢气,故正确;
⑥浓氨水能和硫酸反应生成盐,所以能影响氢气,故错误.
故选A.
点评 本题考查了物质的性质,难度不大,易错选项是②,注意加入KNO3溶液后,相当于溶液中含有硝酸,硝酸和锌反应产生其它气体,这是一个隐含条件,属于易错之处.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:推断题

 .
.
 +4NaOH$\stackrel{△}{→}$2CH3COONa+
+4NaOH$\stackrel{△}{→}$2CH3COONa+ +4H2O.
+4H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,CH(CH3)3的名称为:2-甲基丙烷.
,CH(CH3)3的名称为:2-甲基丙烷.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验顺序 | 加热前/g | 加热后/g |
| 1 | 3.44 | 3.26 |
| 2 | 3.44 | 3.12 |
| 3 | 3.44 | 2.90 |
| 4 | 3.44 | 2.90 |
| 5 | 3.44 | 2.80 |
| 6 | 3.44 | 2.78 |
| 7 | 3.44 | 2.72 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
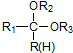 $\stackrel{H+/H_{2}O}{→}$
$\stackrel{H+/H_{2}O}{→}$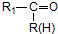
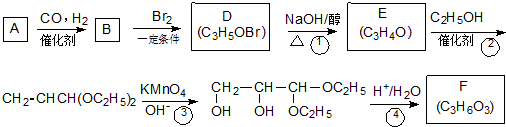
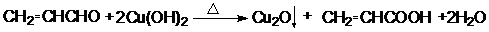 ;
;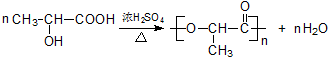 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它的式量为720 | |
| B. | 它是一种单质 | |
| C. | 它是一种新型的共价化合物 | |
| D. | 它在氧气中燃烧的产物和碳在氧气中燃烧的产物相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 其水溶液显强酸性,俗称石炭酸 | |
| B. | 其浓溶液对皮肤有强烈的腐蚀性,如果不慎沾在皮肤上,应立即用NaOH擦洗 | |
| C. | 其在水中的溶解度随温度的升高而增大,超过65℃可以与水以任意比互溶 | |
| D. | 碳酸氢钠溶液中滴入苯酚的水溶液后立即放出二氧化碳 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com