
| A、碳酸钙与稀硝酸反应:CaCO3+2H+═Ca2++CO2↑+H2O |
| B、金属钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ |
| C、铁溶于稀硫酸中:2Fe+6H+═2Fe3++3H2↑ |
| D、氢氧化钡溶液中滴加稀硫酸:Ba2++SO42-═BaSO4↓ |


科目:高中化学 来源: 题型:
A、 向NaOH溶液中加水稀释 |
B、 等质量的Al、Zn与足量的稀硫酸反应 |
C、 向稀硫酸中加入Ba(OH)2溶液 |
D、 恒温下,适量蒸发饱和NaCl溶液的水分 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 常温下,用0.1mol/L NaOH溶液滴定20mL 0.1mol/L CH3COOH溶液的滴定曲线如图.下列说法错误的是( )
常温下,用0.1mol/L NaOH溶液滴定20mL 0.1mol/L CH3COOH溶液的滴定曲线如图.下列说法错误的是( )| A、点①所示溶液中:c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) | ||
| B、点②所示溶液中:c(CH3COOH)>c(Na+)=c(CH3COO-)>c(H+)=c(OH-) | ||
| C、点③所示溶液中:c(Na+)+c(H+)=c(CH3COOH)+c(OH-) | ||
D、在整个滴定过程中:溶液中
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲、乙、丙形成的化合物既有离子键又有共价键 |
| B、乙、丙、丁形成的氢化物常温下均为气体 |
| C、原子序数由小到大顺序为:甲<乙<丙<丁 |
| D、原子半径大小顺序为:丁>甲>乙>丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学键 | C-H | H-H | C-O | C=O | H-O |
| 键能/kJ?mol-1 | a | b | c | d | e |
| HA | H2B | HC | ||
| Ka | Ka1 | Ka2 | Ka3 | Ka4 |
| 数值 | ||||
查看答案和解析>>
科目:高中化学 来源: 题型:
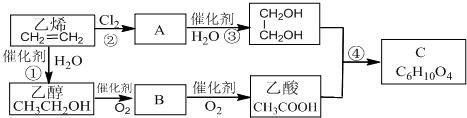
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属X能与NaOH溶液反应放出H2,但金属Y不能,则Y的金属性一定比X弱 |
| B、在合成氨反应达到平衡时,只增加N2的物质的量,达新平衡后N2的百分含量增大 |
| C、在铁件上镀铜时,铁和电源负极相连,铜和正极相连,电解质溶液是CuSO4溶液 |
| D、Cl2和SO2等体积充分混合后,通入品红溶液,溶液颜色没有明显变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SiO2与NaOH溶液:SiO2+2Na++2OH-═Na2SiO3↓+H2O |
| B、将少量SO2气体通入NaClO溶液中:SO2+H2O+2ClO-═SO32-+2HClO |
| C、向含有0.4mol FeBr2的溶液中通入0.1mol Cl2反应:2Fe2++Cl2═2Fe3++2Cl- |
| D、NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com