
| A. | 原子半径 B>D>C | |
| B. | 原子序数 d>c>a | |
| C. | 离子半径 C>D>B | |
| D. | 原子结构的最外层电子数目 B>D>C |
分析 短周期元素的离子aB+、cC3-、dD-都具有相同的电子层结构,结合离子所带电荷,可推知B为Na、C为N、D为F.
A.同周期自左而右原子半径减小、同主族上而下原子半径增大;
B.B、C、D的原子序数分别为11、7、9;
C.电子层结构相同,核电荷数越大,离子半径越小;
D.B、C、D最外层电子数依次为1、5、7.
解答 解:短周期元素的离子aB+、cC3-、dD-都具有相同的电子层结构,结合离子所带电荷,可推知B为Na、C为N、D为F.
A.同周期自左而右原子半径减小、同主族上而下原子半径增大,故原子半径Na>N>F,故A错误;
B.B、C、D的原子序数分别为11、7、9,故原子序数a>d>c,故B错误;
C.电子层结构相同,核电荷数越大,离子半径越小,故离子半径cC3->dD->aB+,故C正确;
D.B、C、D最外层电子数依次为1、5、7,最外层电子数目D>C>B,故D错误,
故选C.
点评 本题考查结构性质位置关系,可以确定元素的相等位置进行解答,但根据短周期元素及离子所带电荷推断元素,利用具体元素更容易进行解答,难度不大.


科目:高中化学 来源: 题型:解答题

| 氢氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
| Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )的废水可以通过构成微生物电池除去,其原理如图所示.
)的废水可以通过构成微生物电池除去,其原理如图所示.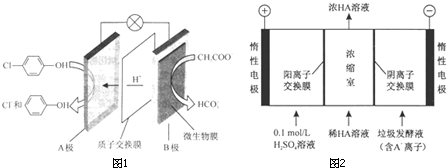
 -OH+2e-+H+═
-OH+2e-+H+═ -OH+Cl-.
-OH+Cl-.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.2g铜与足量稀硝酸反应过程中转移电子0.1NA | |
| B. | 35.5g超氧化钾(KO2)所含的阴离子的数目为NA | |
| C. | 标准状况下将0.5molSO2气体与0.5molH2S气体混合后,气体的分子总数为NA | |
| D. | 6g二氧化硅中含Si-O键数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ①②⑤ | C. | ②③⑥ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴乙烷与NaOH水溶液混合加热后,经冷却,加入硝酸银溶液有淡黄色沉淀 | |
| B. | 淀粉在硫酸作用下水解得到葡萄糖,再加入新制银氨溶液并水浴加热,可得银镜 | |
| C. | 检验溴乙烷消去产物中的乙烯,可将反应逸出的气体直接通入酸性KMnO4溶液中 | |
| D. | 通过核磁共振氢谱的方法,可以检验出溴乙烷在NaOH水溶液中水解的产物有乙醇生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 86 | B. | 136 | C. | 50 | D. | 222 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4g | B. | 25g | C. | 29g | D. | 30g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com