
���� ��1��Mg��OH��2��ˮ��Һ�����ʵ���Ũ����1.65��10-4mol/L����MgO��ˮ��Ӧ���ɵ�c��OH-��=1.65��10-4mol/L��2��1��10-7mol/L����Һ�Լ��ԣ�Ag2O���ܽ����1.6��10-3g/100g����Ag2O��ˮ��Ӧ���ɵ�c��OH-��=$\frac{\frac{1.6��1{0}^{-3}}{232}mol}{0.1L}$��2��1��10-7mol/L����Һ�Լ��ԣ�
��2����NaHCO3ϡ��Һˮ�⣻
�ڼ�����Լ60�棬Mg2+��HCO3-�����ķ�Ӧ���ɳ��������壻
���������¶ȣ��ڷ�ˮԡ�м��ȣ���MgCO3ˮ�����ɼ�����壮
��� �⣺��1��Mg��OH��2��ˮ��Һ�����ʵ���Ũ����1.65��10-4mol/L����MgO��ˮ��Ӧ���ɵ�c��OH-��=1.65��10-4mol/L��2=3.3��10-4mol/L��1��10-7mol/L����Һ�Լ��ԣ�Ag2O���ܽ����1.6��10-3g/100g����Ag2O��ˮ��Ӧ���ɵ�c��OH-��=$\frac{\frac{1.6��1{0}^{-3}}{232}mol}{0.1L}$��2=1.4��10-4mol/L��1��10-7mol/L����Һ�Լ��ԣ�������̪��죬��MgO��Ag2O�ֱ���ˮ�о���ʹ��̪��죬�ʴ�Ϊ����졢��죻
��2���ٻ��ҺpH=7.5����ԭ����HCO3-ˮ���Լ��ԣ��ʴ�Ϊ��HCO3-ˮ���Լ��ԣ�
�ڼ�����Լ60�棬Mg2+��HCO3-�����ķ�ӦΪMg2++2HCO3-$\frac{\underline{\;\;��\;\;}}{\;}$MgCO3��+CO2��+H2O���۲쵽�������ݳ������а�ɫ�������ɣ�
�ʴ�Ϊ���������ݳ������а�ɫ�������ɣ�Mg2++2HCO3-$\frac{\underline{\;\;��\;\;}}{\;}$H2O��
���������¶ȣ��ڷ�ˮԡ�м��ȣ�������MgCO3+H2O$\frac{\underline{\;\;��\;\;}}{\;}$Mg��OH��2+CO2�����۲쵽�������ݳ�����ʹ��̪��죬
�ʴ�Ϊ���������ݳ�����ʹ��̪��죻MgCO3+H2O$\frac{\underline{\;\;��\;\;}}{\;}$Mg��OH��2+CO2����
���� ���⿼�����ܵ���ʵ��ܽ�ƽ�⼰���㣬Ϊ��Ƶ���㣬����Ũ�ȵļ��㼰ˮ�ⷴӦԭ����Ӧ��Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬��Ŀ�Ѷ��еȣ�


 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 A��B��C��D���ֶ�����Ԫ����Ԫ�����ڱ��е����λ����ͼ��ʾ����֪������Ԫ����ֻ��һ���ǽ���Ԫ�أ������ж���ȷ���ǣ�������
A��B��C��D���ֶ�����Ԫ����Ԫ�����ڱ��е����λ����ͼ��ʾ����֪������Ԫ����ֻ��һ���ǽ���Ԫ�أ������ж���ȷ���ǣ�������| A�� | C���Ȼ�����ˮ��Ӧ�������ɰ�ɫ���� | |
| B�� | A���������Ӧ��ˮ����һ��Ϊǿ�� | |
| C�� | D������������Ӧ��ˮ�����ܺ�D���⻯�����Ӧ������ | |
| D�� | ��BԪ�ص�����Һ�еμ�̼��������Һ�����ܲ����ְ�ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ϊ�˼ӿ�����ٶȣ����ò���������������е�Һ�� | |
| B�� | Ϊ�˷�ֹ����ƿ©Һ�����ڲ�������Ϳ�Ϸ�ʿ�� | |
| C�� | Ϊ��ʹ��ȡ���������ʼӿ죬����ϡ�����м�����������ͭ��Һ | |
| D�� | Ϊ��ʹ���Ƶ�FeCl3��Һ���������ǣ��ɼ����������Ƭ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
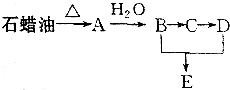 ij����С����ʯ��Ϊԭ�Ͻ�����ͼ��ʾת����ϵ��ʵ��̽��������E���й���ζ���ҷ����к�4��̼ԭ�ӣ�����գ�
ij����С����ʯ��Ϊԭ�Ͻ�����ͼ��ʾת����ϵ��ʵ��̽��������E���й���ζ���ҷ����к�4��̼ԭ�ӣ�����գ� CH3COOCH2CH3+H2O����Ӧ����Ϊ������Ӧ��
CH3COOCH2CH3+H2O����Ӧ����Ϊ������Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ������Ԫ��X��Y��Z��W�����ڱ������λ����ͼ��ʾ��YԪ���ڵؿ��еĺ�����ߣ�����˵����ȷ���ǣ�������
������Ԫ��X��Y��Z��W�����ڱ������λ����ͼ��ʾ��YԪ���ڵؿ��еĺ�����ߣ�����˵����ȷ���ǣ�������| A�� | ԭ�Ӱ뾶��Z��Y��W | |
| B�� | �����̬�⻯������ȶ��ԣ�Y��W | |
| C�� | ��X�Ļ������γɵ���Һһ�������� | |
| D�� | Y����������Ӻ�Z����������Ӻ����������ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | �� MgCl2��Һ�еμ�NaOH��Һ | ���а�ɫ��������Һ�еμ�FeCl3��Һ | ���� |
| ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| ���� | ������ | ������ |
| ���� | ����pH��ֽ���� | ����Һ��pH����7 |
| ���� | ������Һ�еμ���ˮ���ټ���CCl4������ | ��CCl4��ʳ�ɫ |
| ���� | �����������Һ�м���Ba��NO3��2��Һ��ϡHNO3 | ���а�ɫ�������� |
| ���� | �����ˣ�����Һ�м���AgNO3��Һ��ϡHNO3 | ���а�ɫ�������� |
| A�� | �϶����е�������Na+��Br-��SO32- | B�� | �϶�û�е�������Ba2+��SO32- | ||
| C�� | ���ܺ��е�������Cl-��Br-��SO42- | D�� | ����ȷ����������Cl-��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
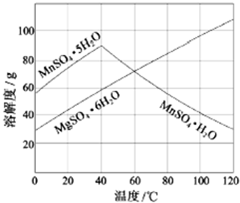 ���̿���Ҫ�ɷ�MnO2�����ʽ���Ԫ��Fe��Al��Mg�ȣ���ˮ����Һ��������SO2��Ӧ���Ʊ�MnSO4•H2O����Ӧ�Ļ�ѧ����ʽΪ��MnO2+SO2=MnSO4
���̿���Ҫ�ɷ�MnO2�����ʽ���Ԫ��Fe��Al��Mg�ȣ���ˮ����Һ��������SO2��Ӧ���Ʊ�MnSO4•H2O����Ӧ�Ļ�ѧ����ʽΪ��MnO2+SO2=MnSO4�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 5�� | B�� | 6�� | C�� | 7�� | D�� | 8�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com