
| 指示剂 | a | b | c |
| 变色pH范围 | 3.1~4.4 | 8.0~10.0 | 4.4~6.2 |
| 说明 | pH<3.1显红色 pH>4.4显黄色 | pH<8.0显无色 pH>10.0显红色 | pH<4.4显红色 pH>6.2显黄色 |
 =0.005cvmol,所以与氨气反应的硫酸的物质的量是0.02mol-0.005cvmol,则与硫酸反应的氨气的物质的量是(0.02mol-0.005cvmol)×2=(0.04-0.01cv)mol。
=0.005cvmol,所以与氨气反应的硫酸的物质的量是0.02mol-0.005cvmol,则与硫酸反应的氨气的物质的量是(0.02mol-0.005cvmol)×2=(0.04-0.01cv)mol。

 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源:不详 题型:问答题
| 编号 | ① | ② | ③ | ④ |
| 装置 | 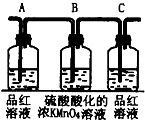 | 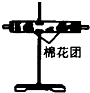 | 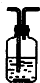 | 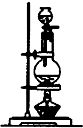 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
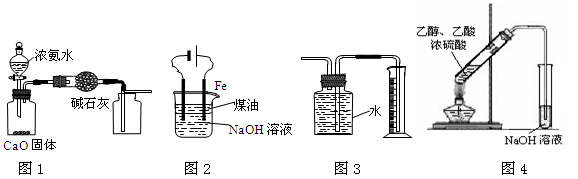
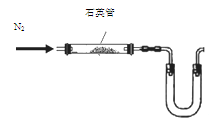
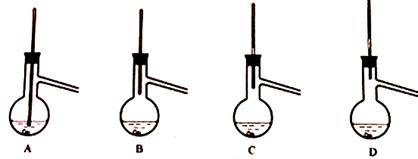
| A.用图1装置制取并收集干燥纯净的NH3 |
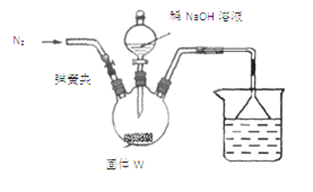
| B.用图2装置实验室制备Fe(OH)2 |
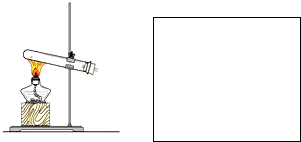
| C.装置3收集并测量Cu与浓硝酸反应产生的气体及体积 |
| D.装置4可用于实验室制取乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
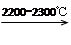 CaC2+CO
CaC2+CO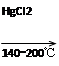 CH2=CHCl
CH2=CHCl查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题


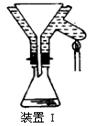
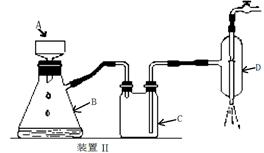

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
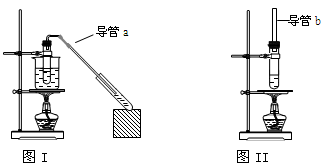
| A.图I装置用于制取乙酸乙酯,图II 装置用于制取乙酸丁酯 |
| B.导管a和导管b的作用都是冷凝回流 |
| C.都可用饱和Na2CO3溶液来洗去酯中的酸和醇 |
| D.加入过量的乙酸可以提高醇的转化率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 编号 | 仪器 | 药品 | 实验目的 |
| A | 托盘天平(带砝码)、250mL容量瓶、量筒、烧杯、药匙、玻玻棒 | NaOH固体、蒸馏水 | 配制250mL一定物质的量浓度的NaOH溶液 |
| B | 分液漏斗、锥形瓶、导管及橡皮塞 | 稀硫酸、碳酸钠、硅酸钠溶液 | 证明非金属性;S>C>Si |
| C | 碱式滴定管、酸式滴定管、胶头滴管、铁架台(带铁夹)、锥形瓶 | 己知浓度的NaOH溶液、待测盐酸、蒸馏水、白纸 | 测定稀盐酸的物质的量浓度 |
| D | 铁架台(带铁夹)、酒精灯、大试管、集气瓶、导管及橡皮塞 | 氯化铵 | 制取氨气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
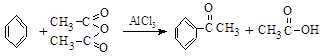

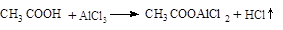 等副反应。
等副反应。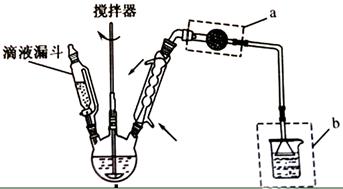
| A.反应太剧烈 | B.液体太多搅不动 | C.反应变缓慢 | D.副产物增多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com