
在实验室利用下列装置,可制备某些气体并验证其化学性质.
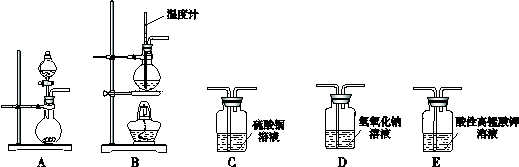
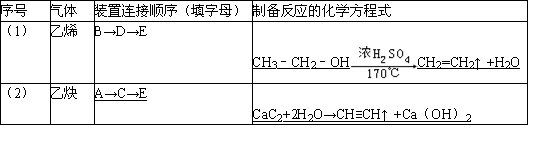
完成下列表格:
 (3)D装置中氢氧化钠溶液的作用 .
(3)D装置中氢氧化钠溶液的作用 .
考点:实验装置综合.
专题:实验设计题.
分析:(1)实验室制取乙烯,需要加热到170℃,应该选择B装置,反应中会发生副反应生成二氧化硫,必须用氢氧化钠溶液除去,所以选择D装置除质;最后用高锰酸钾溶液检验乙烯的性质;
(2)碳化钙与与水反应生成乙炔,选A为反应装置,然后选C为除杂装置,选E为性质实验装置;
(3)NaOH溶液的作用为除去.
解答: 解:(1)在实验室中制取乙烯,需要加热到170℃,应该选择B装置,反应中会发生副反应生成二氧化硫,必须用氢氧化钠溶液除去,所以选择D装置除去二氧化硫、二氧化碳杂质;最后用高锰酸钾溶液检验乙烯的性质,所以连接顺序为:B→D→E,实验室利用乙醇能发生消去反应制乙烯的反应为CH3﹣CH2﹣OH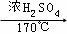 CH2=CH2↑+H2O,
CH2=CH2↑+H2O,
故答案为:CH3﹣CH2﹣OH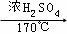 CH2=CH2↑+H2O;
CH2=CH2↑+H2O;
(2)碳化钙与与水反应生成乙炔,选A为反应装置,然后选C为除杂装置,选E为性质实验装置,则装置的顺序为A→C→E,制备乙炔的反应为CaC2+2H2O→CH≡CH↑+Ca(OH)2,故答案为:A→C→E;CaC2+2H2O→CH≡CH↑+Ca(OH)2;
(3)由(1)可知,D装置中氢氧化钠溶液的作用是除二氧化碳和二氧化硫,故答案为:除二氧化碳和二氧化硫.
点评:本题考查实验装置综合和气体的制备,为高频考点,把握制备原理及实验装置的作用为解答的关键,侧重分析及实验能力的考查,题目难度不大.


科目:高中化学 来源: 题型:
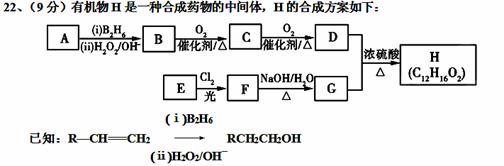
请回答下列问题:
(1)A为质谱图中最大质荷比为104的芳香烃,A的分子式为________。
(2)上述所有反应中属于取代反应的有 个
(3)C 物质中碳元素的杂化方式有: F为一氯代物,其核磁共振氢谱有三个吸收峰,则E的结构简式为________。
(4)写出B→C的化学方程式:________。
(5)写出D和G生成H的化学方程式:________。
(6)D的同分异构体中能与FeCl3溶液发生显色反应且能发生银镜反应的有________种,写出其中核磁共振氢谱中吸收峰数目最少的结构简式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验装置的说法中正确的是( )
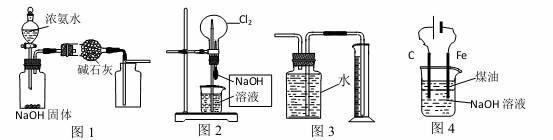
A.图1装置可制取干燥纯净的NH3
B.图2装置可以完成“喷泉”实验
C.图3装置可测量Cu与浓硝酸反应产生气体的体积
D.图4装置可用于实验室制备Fe(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
五种短周期元素A、B、C、D、E原子序数依次增大,结合下列信息:
(1)A原子核外电子总数是内层电子数的三倍,A、E同主族;
(2)B的最高价氧化物对应的水化物F与其气态氢化物G反应,得到离子化合物H;
(3)C的焰色反应呈黄色;
(4)D在同周期主族元素形成的简单离子中,离子半径最小.回答下列问题:
(1)写出D在元素周期表中的位置: ;
(2)化合物H的水溶液pH 7,其原因是 NH(用离子方程式表示);
(3)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其他四种物质发生化学反应,写出该物质的电子式 ;
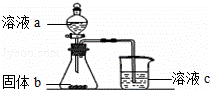
(4)某同学设计实验证明A、B、E的非金属性强弱关系.设计如图装置:
①溶液a和固体b分别为 , ;
②该装置有一个明显不足是 ;若装置改进后溶液c中发生反应的离子方程式为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中需要配制2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取NaCl质量分别是 ( )
A.950mL,111.2g B.500mL,117g C.1000mL,117g D.1000mL,111.2g
查看答案和解析>>
科目:高中化学 来源: 题型:
配制0.1mol•L﹣1的NaCl溶液,下列操作会导致所配溶液的物质的量浓度偏高的是( )
A.称量时,左盘高,右盘低 B.定容时俯视读取刻度
C.原容量瓶洗净后未干燥 D.定容时液面超过了刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com