
| A、Na2CO3+HCl |
| B、BaCO3+HCl |
| C、K2CO3+HNO3 |
| D、Na2CO3+H2SO4 |


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
| pH t/min T/℃ | 10.0 | 9.0 | 8.0 | 7.0 |
| 15 | 30 | 24 | 16 | 6 |
| 20 | 18 | 13 | 8 | 4 |
| 25 | 12 | 8 | 5 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同浓度的下列溶液中:①(NH4)2Fe(SO4)2 ②(NH4)2CO3 ③(NH4)2SO4,c(NH4+)由大到小的顺序是:①>③>② |
| B、常温时,将等体积的盐酸和氨水混合后,pH=7,则c(NH4+)>c(Cl-) |
| C、0.2mol?L-1Na2CO2溶液中:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3) |
| D、0.1 mol?L-1的NH4Cl溶液与0.05mol?L-1NaOH溶液等体积混合:c(Cl-)>c(NH4+)>c(Na+)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol?L-1NaCl与0.05mol?L-1Na2CO3溶液中的Na+离子数目 |
| B、质量相等的金刚石和C60中的碳原子数目 |
| C、标准状况下等体积的SO2与SO3的分子数目 |
| D、pH都为3的稀盐酸与FeCl3溶液中,由水电离产生的H+离子数目 |
查看答案和解析>>
科目:高中化学 来源: 题型:
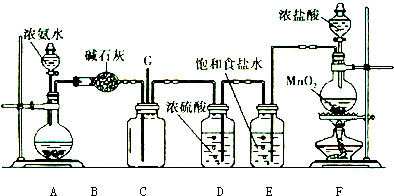
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在0℃,101kPa,1mol SO3中含有NA个硫原子 |
| B、1mol C8H18分子中含有的共用电子对数为26NA |
| C、0.5L 0.1mol/L NH4Cl溶液中含NH4+离子的数目为0.05NA |
| D、反应KClO3+6HCl═KCl+3Cl2↑+3H2O中,每生成1mol Cl2转移的电子为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将BaSO4放入水中不能导电,所以BaSO4是非电解质 |
| B、氨溶于水得到的氨水能导电,所以氨水是电解质 |
| C、固态的离子化合物不导电,熔融态的离子化合物导电 |
| D、强电解质溶液的导电能力一定比弱电解质溶液的导电能力强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.8g NH4+含有的电子数为NA |
| B、1mol Cl2与足量Fe反应,转移的电子数为3NA |
| C、46g的NO2与46g的N2O4含有的原子数不同 |
| D、标准状况下11.2L苯完全燃烧产生二氧化碳分子数为3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com