
����Ŀ����ʳ��Ϊԭ�Ͻ����������ۺ����õ�ijЩ������ͼ1��ʾ�� 
��1����ȥ�����е�Ca2+��Mg2+��SO42�����ӣ��������г�������˳���ǣ�����ţ� ��
a��Na2CO3 b��NaOH c��BaCl2
��2������Һ��pH�������Գ�ȥ�������� ��
��3��ͼ2��ʾ��ⱥ��NaCl��Һ��װ�ã�X��Y��ʯī����ʵ�鿪ʼʱ��������ͬʱ�����뼸�η�̪��Һ����ش��������⣺X���ϵĵ缫��Ӧʽ�� �� ��X�������۲쵽����������Y�缫�ϵĵ缫��Ӧʽ�� �� ����õ缫��Ӧ����ķ����� �� ���NaCl��Һ�����ӷ���ʽ�� ��
��4����������NaHCO3������ĸҺ�м��������ʯ�ң���ɻ��һ�ֿ���ѭ��ʹ�õ����壬�仯ѧʽ�� ��
��5�������£���ijpH=11��Na2CO3��Һ�м������ʯ���飬���˺�������ҺpH=13����Ӧǰ����Һ���뷴Ӧ�����Һ��ˮ�������c��OH�����ı�ֵ�� ��
���𰸡�
��1��cab����cba����bca
��2��OH����CO32��
��3��2H++2e��=H2��������ɫ���ݲ�������Һ��죻2Cl����2e��=Cl2������ʪ���KI������ֽ����������ڣ����۲쵽��ֽ������֤����Cl2������2Cl��+2H2O ![]() 2OH��+H2��+Cl2��
2OH��+H2��+Cl2��
��4��NH3
��5��1��1010
���������⣺��1.����������������Һʱ���ܺ��Ȼ�þ��Ӧ����������þ�������Ȼ��ƣ��Ӷ���ȥ�Ȼ�þ�������Ȼ���ʱ���ܺ������Ʒ�Ӧ�������ᱵ�������Ȼ��ƣ��Ӷ���ȥ�����ƣ�����̼������Һʱ���ܺ��Ȼ��ơ��������Ȼ�����Ӧ����̼��Ƴ�����̼�ᱵ�������Ȼ��ƣ��Ӷ���ȥ�Ȼ��ƺ������Ȼ��������ˣ�����Һ�м���������ϡ����ʱ�����ѹ������������ƺ�̼���Ƴ�ȥ���Դ����ƣ�������μ����Ȼ�����Һ������������Һ��̼������Һ�����μ����Ȼ�����Һ��̼������Һ������������Һ�����Դﵽͬ����Ŀ�ģ����Դ��ǣ�cab����cba����bca��
��2.��ϡ�����ܺ��������ơ�̼���Ʒ�Ӧ������ʱ���Եõ��Ȼ��Ƶı�����Һ������Һ��pH�������Գ�ȥ��������OH����CO32�� �� ���Դ��ǣ�OH����CO32����
��3.���͵�Դ�ĸ����������ǵ��ص��������õ缫�ϵĵ缫��ӦΪ��2H++2e��=H2����������Ũ�ȼ�С�����Լ�����ǿ����̪��죬�͵�Դ���������������������û���ӦʽΪ��2Cl����2e��=Cl2�������������ķ���Ϊ����ʪ���KI������ֽ����������ڣ����۲쵽��ֽ������֤����Cl2���������������ϵĵ缫��Ӧ���Եõ��ܷ�ӦΪ��2Cl��+2H2O ![]() 2OH��+H2��+Cl2�������Դ��ǣ�2H++2e��=H2��������ɫ���ݲ�������Һ��죻2Cl����2e��=Cl2������ʪ���KI������ֽ����������ڣ����۲쵽��ֽ������֤����Cl2������2Cl��+2H2O
2OH��+H2��+Cl2�������Դ��ǣ�2H++2e��=H2��������ɫ���ݲ�������Һ��죻2Cl����2e��=Cl2������ʪ���KI������ֽ����������ڣ����۲쵽��ֽ������֤����Cl2������2Cl��+2H2O ![]() 2OH��+H2��+Cl2����
2OH��+H2��+Cl2����
��4.�������NaHCO3������ĸҺ�к����Ȼ�泥����������ʯ�Һ������ƺ�ˮ��Ӧ�����������ƣ��������ƺ��Ȼ�立�Ӧ�������Ȼ��ơ�ˮ�Ͱ�������������ѭ��ʹ�ã���ѧʽ��NH3 �� ���Դ��ǣ�NH3��
��5.��pHΪ11̼������Һ�У�C��H+��ʣ��C��OH����ˮ=10��14��C��OH����ˮ=10��3mol/L��Na2CO3��Һ�м������ʯ���飬��Ӧ����̼��ƺ��������ƣ�������ҺpH=13�����ʱˮ�������c��OH������ֵ��10��13mol/L�����Է�Ӧǰ����Һ���뷴Ӧ�����Һ��ˮ�������c��OH�����ı�ֵ�� ![]() =1��1010 �� ���Դ��ǣ�1��1010 ��
=1��1010 �� ���Դ��ǣ�1��1010 ��


 ��ڽ��ȫ������ϵ�д�
��ڽ��ȫ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����÷�Ӧ6NO2+8NH3�T7N2+12H2O���ɵ�صķ���������ʵ����Ч��������������ŷţ����ỷ����Ⱦ�����ܳ�����û�ѧ�ܣ�װ����ͼ��ʾ������˵������ȷ���ǣ� �� 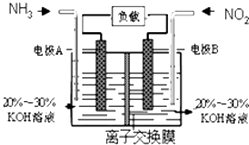
A.�������Ҳ�缫�������غ��������缫
B.Ϊʹ��س����ŵ磬���ӽ���Ĥ��ѡ�������ӽ���Ĥ
C.�缫A����ӦʽΪ��2NH3��6e��=N2+6H+
D.����4.48L NO2����״���� ������ʱ��ת�Ƶ���Ϊ0.8mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������з�Ӧ������д����Ӧ�����ӷ���ʽ��
(1)��FeCl3��Һ�еμ�NaOH��Һ������__________________�����ӷ���ʽ��____________________
(2)��NaHCO3��Һ�еμ�ϡH2SO4������__________________�����ӷ���ʽ��__________________
(3)ϡHNO3��Ba(OH)2��Һ��ϣ�����__________________�����ӷ���ʽ��____________________
(4)�Ƚϣ������������ӷ�Ӧ�����������IJ�ͬ����______________________����ͬ����________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������̫���ֽܷ�ˮ���ɵ������ڴ����������������̼��Ӧ���ɼ״���ˮ�����������Լ״�Ϊȼ�ϵ�ȼ�ϵ�أ���֪ͼ�׳�Ϊ�״�ȼ
�ϵ�أ��ҳ��е������缫��Ϊʯī�缫���ҳ���ʢ��100mL 3.00mol��L��1��CuSO4��Һ����ش��������⣺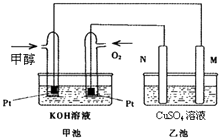
��1��M�ĵ缫��ӦʽΪ
��2�����ҳ���ijһ�缫��������ͭ6.4gʱ���׳�����������������Ϊ����L������״����
��3�����ҳ������缫����������ǡ�����ʱ�������״���£�����������ͨ��g�״���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʷ��ӣ������ӣ���ˮ����������ˮ����ɢ��______������______�仯��
A.���գ���ѧB.�ų�������
C.���գ�����D.�ų�����ѧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��T��Q��R��W��Ԫ�����ڱ��е�λ����ͼ��ʾ������T����������������������������ȣ����ǵ�����������ˮ��������Ϊ�ס��ҡ���������������������ȷ���ǣ� �� 
A.R���⻯����Լ��м��Լ����зǼ��Լ�
B.�����¶���Ũ��Һ����T�������Ƶ�������ʢװ
C.����Ũ��Һ��Q�ĵ��ʼ��ȷ�����Ӧ�������������Ϊ1��2����������
D.�ס��ҡ����������Ⱦ��ֽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��CO2+Ca(OH)2![]() CaCO3��+H2O��CaCO3+CO2+H2O
CaCO3��+H2O��CaCO3+CO2+H2O![]() Ca(HCO3)2����Ca(HCO3)2������ˮ���Ը�����ͼ��ʾװ�ûش��������⣺
Ca(HCO3)2����Ca(HCO3)2������ˮ���Ը�����ͼ��ʾװ�ûش��������⣺
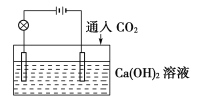
(1)ͨ��CO2ǰ������________(�����������)��
(2)��ʼͨ��CO2ʱ�����ݵ�����________��
(3)����ͨ�������CO2�����ݵ�����________��
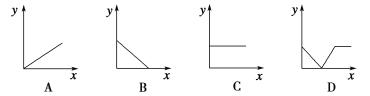
(4)�����ĸ�ͼ�У�_______(����ĸ)�ܱȽ�ȷ�ط�ӳ����Һ�ĵ���������ͨ��CO2�������Ĺ�ϵ(x���ʾCO2ͨ�������y���ʾ��������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ұ����������ڷ�������л��������һ�����ʣ���ת���������£� 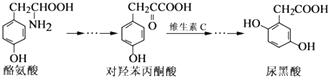
����˵��������ǣ� ��
A.�Ұ�����������ᷴӦ���������������Ʒ�Ӧ
B.1 mol�����������Ũ��ˮ��Ӧ���������3 mol Br2
C.���ǻ�����ͪ���������ͬһƽ���ϵ�̼ԭ��������7��
D.1 mol�����������NaHCO3��Ӧ���������3 mol NaHCO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�������Ҫ�ò����������в�����������ͬ����( )
�ٹ��� ������ ��������ƿת��Һ��
A. �ٺ͢� B. �ٺ͢� C. �ں͢� D. �٢ڢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com